MP Board Class 8th Science Solutions Chapter 12 Friction
MP Board Class 8th Science Friction NCERT Textbook Exercises
Mp Board Class 8 Science Chapter 12 Question 1.
Fill in the blanks:
(a) Friction opposes the …………. between the surfaces in contact with each other.
(b) Fraction depends on the …………… of surfaces.
(c) Friction produces …………….. .
(d) Sprinkling of powder on the carrom board …………. friction.
(e) Sliding friction is ……………. than the static friction.
Answer:
(a) relative motion
(b) nature
(c) heat
(d) reduces
(e) less.
Mp Board Class 8 Science Solution Chapter 12 Question 2.
Four children were asked to arrange forces due to rolling, static and sliding frictions in a decreasing order. Their arrangements are given below. Choose the correct arrangement.
(a) Rolling, static, sliding.
(b) Rolling, sliding, static
(c) Static, sliding, rolling
(d) Sliding, static, rolling.
Answer:
(c) Static, sliding, rolling
Class 8 Science Chapter 12 Mp Board Question 3.
Alida runs her toy car on dry marble floor, wet marble floor, newspaper and towel spread on the floor. The force of friction acting on the car on different surfaces in increasing order will be:
(a) Wet marble floor, dry marble floor, newspaper and towel.
(b) Newspaper, towel, dry marble floor, wet marble floor.
(c) Towel, newspaper, dry marble floor, wet marble floor.
(d) Wet marble floor, dry marble floor, towel, newspaper.
Answer:
(a) Wet marble floor, dry marble floor, newspaper and towel.
Mp Board Class 8 Social Science Solution Chapter 12 Question 4.
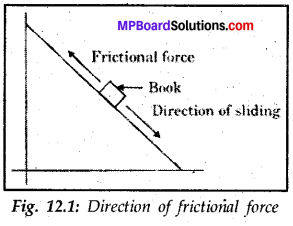
Suppose your writing desk is tilted a little. A book kept on it starts sliding down. Show the direction of frictional force acting on it.
Answer:
The frictional force will act parallel to the inclined surface, opposite to the direction of the sliding of book.
Mp Board Class 8 Social Science Chapter 12 Question 5.
You spill a bucket of soapy water on a marble floor accidentally. Would it make it easier or more difficult for you to walk on the floor? Why?
Answer:
It is difficult to walk on a soapy floor because layer of soap makes floor smooth. The coating of soap reduces the friction and the foot cannot make a proper grip on the floor and it starts getting to slip on the floor.
Mp Board Solution Class 8 Science Chapter 12 Question 6.
Explain why sportsmen use shoes with spikes?
Answer:
Sportsmen use shoes with spikes to increase the friction so that their shoes do not slip while they run or play.
Mp Board Class 8 Science Solution Chapter 11 Question 7.
Iqbal has to push a lighter box and Seema has to push a similar heavier box on the same floor. Who will have to apply a larger force and why?
Answer:
Seema will experience more frictional force because the heavy object will be pressed hard against the opposite surface and produces more friction.
Class 8 Science Chapter 12 Question Answer Question 8.
Explain why sliding friction is less than the static friction.
Answer:
When the box starts sliding, the contact points on the surface of the box do not get enough time to lock into the contact points of the floor. Hence, the sliding friction is slightly less than the static friction. This is why the sliding friction is always less than the static friction.
Class 8 Science Chapter 12 Question 9.
Give examples to show that friction is both a friend and a foe.
Answer:
Friction is a friend because:
- We cannot imagine to be able to walk without friction.
- We cannot write with pen or pencil in absence of friction.
- The automobiles could not be started or stopped or turned to change the direction of motion if there were no friction between the tyres of the vehicle and the surface of the road.
- We cannot fix a nail in the wall or tie a knot if there is no friction.
- No building could be constructed without friction.
Friction is a foe because:
- It wears out the materials such as shoes, screws and ball bearings.
- Friction causes heat. When a machine. is operated, heat generated causes much wastage of energy. Thus, Friction acts as a friend as well as a foe. Also, friction is a necessary evil.
Mp Board Solution Class 8 Question 10.
Explain why objects moving in fluids must have special shapes.
Answer:
When objects move through fluids, they have to overcome the friction acting on them. Efforts are therefore made to minimize the friction so objects are given special shapes. Idea of such shapes come from the body structure of birds and fishes which have to move about in fluids all the time. Such shapes are called streamlined. Giving such shapes to the ships, planes and cars is called streamlining.
MP Board Class 8th Science Friction NCERT Extended Learning – Activities and Projects
Question 1.
What role does friction play in the sport of your choice? Collect some pictures of that sport in action where friction is either supporting it or opposing it. Display these pictures with proper captions on the bulletin board of your classroom.
Answer:
Do yourself.
Question 2.
Imagine that friction suddenly vanishes. How would the life be affected. List ten such situations.
Answer:
Do yourself.
Question 3.
Visit a shop which sells sports shoes. Observe the soles of shoes meant for various sports. Describe your observations.
Answer:
Do yourself.
Question 4.
A toy to play with:
Take an empty matchbox. Take out its tray. Cut a used refill of a ball pen of the same width as the tray as shown in the figure below. Fix the refill with two pins on the top of the tray as shown in Fig. 12.2. Make two holes on the opposite sides of the tray. Make sure that the holes are large enough to allow a thread to pass through them easily. Take a thread about a metre long and pass it through the holes as shown. Fix beads at the two ends of the thread so that it does not come out. Insert the tray in the outer cover of the matchbox. Suspend the match box by the thread. Leave the thread loose. The match box will start falling down due to gravity. Tighten the thread now and observe what happens. Explain your observation. Can you relate it to friction?

Answer:
Do yourself.
MP Board Class 8th Science Friction NCERT Additional Important Questions
A. Short Answer Type Questions
Question l.
What is friction?
Answer:
The force acting equal and opposite surfaces? Does it depend on the smoothness to the relative motion of two objects in of the surface?
contact is known as friction.
Question 2.
How is friction caused? the surfaces. Yes, it depends on the
Answer:
Friction is caused by the irregularities smoothness of the surface. It is the least on the two surfaces in contact. the smoothest surface.
Question 3.
In which direction does friction work? Smooth surfaces provide less friction, whereas
Answer:
Frictions works opposite to the motion, rough surfaces provide more friction.
Question 4.
Is the friction the same for all the
Answer:
No, friction is not the same for all
B. Long Answer Type Questions
Question 5.
Why does the friction between two
Answer:
Since the friction is due to the interlocking of irregularities in the two surfaces which slide with respect to each other, it is obvious that the force of friction will increase if the two surfaces are pressed harder. One can experience it by dragging a mat when nobody is sitting on it and when a person is sitting on it.
Question 6.
What would happen if there were no force of friction? Imagine and describe in your own words.
Answer:
If there were no friction, many problems could have been arise. One cannot able to walk if there were no friction at all. One could not write with pen or pencil, if there were no friction. When one is writing with chalk on the blackboard, its rough surface rubs off some chalk particles. So, we can se the writing on the black board. If any object just started moving, it would never stop. Had there been no friction between the tyres of the automobiles and the road, they could not be started or stopped or turned to change the direction of motion. One could not fix a nail in the wall or knot. Also, without friction no building could so constructed.
Question 7.
It is easy to move an object on a sliding surface than the plane surface. Why?
Answer:
Every surface has some irregularities on it. On a plane surface these irregularities get interlocked easily and it becomes a little hard for the object to move. In case of sliding surfaces, the irregularities do not get enough time to interlock, so the object moves easily on the sliding surface.
Question 8.
Why is friction called an evil?
Answer:
Friction is an evil. It causes a lot of problems for us. It wears out the objects or materials on which it acts. The soles of our shoes get worn due to friction. The floors, machines, their parts, clothes, metals etc., get weared due to the friction they bear. Friction spoils the parts of the machines. They are, therefore, regularly lubricated to minimise friction. Friction produces heat, which further damages the objects on which it is exerted. The grooves of the tyres are finished due to regular friction they bear, which is offered by their regular motion on roads. Except this wear and tear, friction utilize a large amount of energy spent to overcome it.