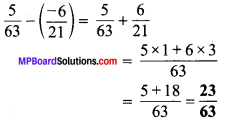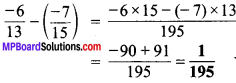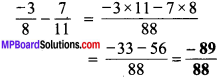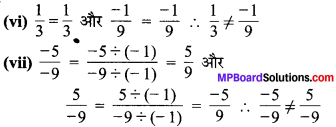MP Board Class 9th Sanskrit Solutions Durva Chapter 21 सूक्तयः (स्फुट)
MP Board Class 9th Sanskrit Chapter 21 पाठ्य पुस्तक के प्रश्न
प्रश्न 1.
एक पदेन उत्तरं लिखत (एक शब्द में उत्तर लिखो)
(क) सत्य क्षमाभ्यां कस्य सिद्भिः? (सत्य के क्षमाभ्यास से किसकी सिद्धि होती है?)
उत्तर:
सकलार्थः। (सभी प्रकार की)
(ख) मे मनः कीदृशः अस्तु? (मेरः मन किस तरह का हो?)
उत्तर:
शिव संकल्पमस्तु। (शिव संकल्प वाला हो)।।
(ग) कर्मसु कौशलम् किम्? (कर्म में कुशलता किससे आती है?)
उत्तर:
योगः। (योग से)
![]()
(घ) प्रमाद कस्मात् न कर्त्तव्यः? (किसमें प्रमाद नहीं करना चाहिए?)
उत्तर:
स्वाध्याय। (स्वाध्याय में)
(ङ) कः रक्षितः रक्षति? (किसकी रक्षा ही रक्षा है?)
उत्तर:
धर्मा। (धर्म की)
प्रश्न 2.
एक वाक्येन उत्तर लिखत (एक वाक्य में उत्तर लिखो)
(क) सर्वारम्भः कः? (सबसे पहले क्या आरम्र होता है?)
उत्तर:
सर्वारम्भा मन्त्रमूलाः। (सबसे पहले मूल मंत्र आरंभ होता है।)
(ख) नरः कथं सुखी भवति? (व्यक्ति सुखी कैसे होता है?)
उत्तर:
नरः आहारे व्यवहारे च त्यक्तलज्जः सुखी भवेत्। (जो व्यक्ति भोजन और शिष्टाचार में लज्जा को त्यागने वाला है, वही सुखी रहता है)
(ग) सकलं कदा नष्टं भवति? (सम्पूर्ण कब नष्ट हो जाता है?)
उत्तर:
यदि आचरणं मलिनं भ्रष्टम् तदा सकलं नष्टं भवति। (यदि आचरण सन्तोषप्रद नहीं है तो सम्पूर्ण नष्ट हो जाता है।)
प्रश्न 3.
उचितमेलनं कुरुत-

प्रश्न 4.
रेखांवित शब्दार आधृत्य प्रश्ननिर्माणं कुरुत
(क) धर्मो रक्षितः रक्षति
प्रश्न : धर्मों कः रक्षति?
(ख) भ्रष्टाचारण सर्वं नष्टंपति।
प्रश्न : केन आचरेण सर्वं नष्टं भवति?
(ग) द्यिा मुक्तिप्रदा अस्ति।
प्रश्न : विद्या का अस्ति?
प्रश्न 5.
रक्तस्थानानि पूरयत
(श) सा विद्या या विमुक्तये।
(ष) स्वाध्याय न प्रमदितव्यम्।
(स) आहारे व्यवहारे च त्यक्तलज्जः सुखी भवेत्।।
(ह) सत्यश्रमाभ्याम् सकलार्थ सिद्धिः।
प्रश्न 6.
सन्धि विच्छेदं कुरुत-
तन्न – तत्+न।
धर्मोरक्षति – धर्मः+रक्षति।
स्वाध्यायान्मा – स्वाध्याय+अयान्मा।
![]()
प्रश्न 7.
कोष्ठकात् शब्द चित्वा सूक्तिं रचयत
धर्मो, योगः, यत्र, सकलम्
यथा-
धर्मो – धर्मो रक्षति रक्षितः।
योगः – योगः कर्मसु कौशलम्।
यत्र – यत्र नारयस्तु पूजयन्ते रमन्ते तत्र देवता।
सकलम् – सत्यश्रमाभ्याम् सकलार्थ सिद्धिः।
प्रश्न 8.
सूक्त्या पूर्ति करोतु-(सूक्ति द्वारा)
प्रश्न 9.
संस्कृतवाक्येषु प्रयोगं कुरुत
यत्र, तत्र, हि, च, या
यत्र – यत्र धूम्रः तत्र अग्नि।
तत्र – तत्र खगाः सन्ति।
हि – मानो हि महताम धनम।
च – अन्नं, जलं च सुभाषितम् पृथ्वियां श्रेष्ठः रत्नाः सन्ति।
या – सा विद्या या विमुक्तये।
प्रश्न 10.
समानार्थक शब्दं लिखत
लज्जा – व्रीड़ा
ल कष्टं – दुःखं
स्वाध्याय – अध्ययनम्।
प्रश्न 11.
अधोलिखित प्रश्नानाम् उत्तराणि लिखत-
(क) योगस्याशयः स्पष्टं करोतु?
उत्तर:
कर्मस्य कौशलम्।।
(ख) कुत्र कुत्र प्रमादः न कर्त्तव्यम्?
उत्तर:
देव पितृकार्याभ्यां।
(ग) धर्मः कथं रक्षति?
उत्तर:
सर्व प्रकारेण, धर्म क्षेत्रे, कर्म क्षेत्रे धर्मः रक्षति।
(घ) कीदृशी विद्या मुक्तिं ददाति?
उत्तर:
तपः शालिनी विद्या मुक्तिं ददाति।
(ङ) भ्रष्टाचारेण किं किं भवति?
उत्तर:
भ्रष्टाचारेण सर्वं नष्टं भवति।
![]()
सूक्तयः पाठ-सन्दर्भ/प्रतिपाद्य
सुंदर उक्ति अर्थात् कथन ही सूक्ति कहलाता है। अनुभव पूर्ण हितकारक वचन ही सूक्ति कहलाता है। सूक्ति मानव स्वभाव को शोध कर सन्मार्ग पर अग्रसर करती है और श्रेष्ठ आचार-व्यवहार का उपदेश देती है। अतः शिक्षण में भी सूक्तियों का विशेष महत्त्व है। प्रस्तुत पाठ में विभिन्न ग्रन्थों से सूक्तियों का संकलन कर यहाँ प्रस्तुत किया गया है।
शब्दार्थ :
सत्यश्रमाभ्याम्-सत्य और श्रम द्वारा-through truth and labour; विमुक्तये-मुक्ति के लिए-for finished for the freedom; प्रमदितव्यम्-प्रमाद करना चाहिए-intoxication self; रमन्ते-निवास करते हैं-lives; सर्वारम्भाः-सभी कार्यों का आरम्भ-start of all work; अन्तःकरणम्-मन बुद्धि आदि-mind, wisdom; भव-होओ (हे)-happen; देवपितृकार्याभ्यां-देव और पितृ कार्यों में-God and sons work; प्रमदः-आलस्य-Ideal;,laziness; त्यक्त लज्जः-जिसने लज्जा को त्याग दिया हो-wicked; वस्तुषु-वस्तुओं में-In things;सुखी भवेत्-सुखी होता है-Happy;शक्यं-शक्ति-power.
सूक्तयः पाठ का हिन्दी अर्थ
1. मे मनः शिवसङ्कल्पमस्तु।
मेरा मन शुभ संकल्प वाला हो।
2. सत्यश्रमाभ्याम् सकलार्थः सिद्धिः।
सत्य एवं परिश्रम से सकलार्थ (सभी कार्यों की) सिद्धि होर्तः है।
3. सा विद्या या विमुक्तये।
विद्या वह है जो मुक्ति प्रदान करे।
4. ये.गः कर्मसु कौशलम्।
योग से कर्म करने की कुशलता आती है।
5. स्वाध्यायान्मा प्रमदः।
स्वाध्याय में प्रमाद न करें।
![]()
6. देवपितृकार्याभ्यां न प्रमदितव्यम्।
देव और पितृकार्य में भी आलस्य न करें।
7. धर्मो रक्षति रक्षितः।
धर्म की रक्षा से ही स्व रक्षा होती है।
8. मन्त्रमूलाः सर्वारम्भाः।
सभी कार्यों का मूल मंत्र प्रारंभ करना है।
9. आहारे व्यवहारे च त्यक्तलज्जः सुखी भवेत्।
भोजन और शिष्टाचार में लज्जा का त्याग करने वाला ही सुखी रहता है।
10. सतां हि सन्देहपदेषु वस्तुषु प्रमाणमन्तःकरणप्रवृत्तयः।
संदेह होने पर अंतःकरण की वृत्ति ही प्रमाण होती है।
11. सकलं कष्टं निखिलं नष्टं यदि आचरणं मलिनं भ्रष्टम्।
यदि आचरण दूषित हो तो वह समस्त कष्टों को देने वाला है एवं सम्पूर्ण को नष्ट करके वाला होता है।
12. उपायेन हि यच्छक्यं तन्न शक्यं पराक्रमः।
उपाय से ही यथा शक्ति पराक्रम प्राप्त होता है।