MP Board Class 11th Chemistry Solutions Chapter 6 ऊष्मागतिकी
ऊष्मागतिकी NCERT अभ्यास प्रश्न
प्रश्न 1.
ऊष्मागतिकी अवस्था फलन एक राशि है –
(a) जो ऊष्मा-परिवर्तनों के लिए प्रयुक्त होती है।
(b) जिसका मान पथ पर निर्भर नहीं करता है।
(c) जो दाब-आयतन कार्य की गणना करने में प्रयुक्त होती है।
(d) जिसका मान केवल ताप पर निर्भर करता है।
उत्तर:
(b) क्योंकि अवस्था फलन केवल प्रारंभिक तथा अंतिम अवस्था पर निर्भर करते है।
प्रश्न 2.
एक प्रक्रम के रुद्धोष्म परिस्थितियों में होने के लिए –
(a) ∆T = 0
(b) ∆P = 0
(c) q = 0
(d) W = 0.
उत्तर:
(c) रुद्धोष्म प्रक्रम में न तो ऊर्जा निकलती है और न ही अवशोषित होती है अतः q= 0.
प्रश्न 3.
सभी तत्वों की एन्थैल्पी उनकी सन्दर्भ-अवस्था में होती है –
(a) इकाई
(b) शून्य
(c) < 0
(d) सभी तत्वों के लिए भिन्न होती है।
उत्तर:
(b) शून्य
प्रश्न 4.
मेथेन के दहन के लिए ∆U° का मान – X kJ mol-1 है। इसके लिए ∆H° का मान होगा –
(a) = ∆H°
(b) > ∆U°
(c) < ∆U°
(d) = 0
उत्तर:
CH2(g)A + 2O2(g) → CO2(g) + 2H2O(l)
∆ng = 1 – 3 = – 2
∆H = ∆U + ∆ngRT = ∆U – 2RT
∆H < ∆U
∴ सही उत्तर (c).
प्रश्न 5.
मेथेन, ग्रेफाइट एवं डाइहाइड्रोजन के लिए 298 K पर दहन एन्थैल्पी के मान क्रमशः -890.3 kJ mol-1 -393.5 kJ mol-1 एवं – 285.8 kJ mol-1 हैं। CH4(g) की विरचन एन्थैल्पी क्या होगी –
(a) – 74.8 kJ mol-1
(b) – 52:27 kJ mol-1
(c) + 74.8 kJ mol-1
(d) +52-26 kJ mol-1
उत्तर:
दिया गया है-
(i) CH4(g) + 2O2(g) → CO2(g) + 2H2O; ∆H = -890.3 kJ mol-1
(ii) C(s) + O2(g) → CO2(g); ∆H = -393.5 kJ mol-1.
(iii) H(s) ) + 5O2(g) → H2O(l); ∆H = -285.8 kJ mol-1.
आवश्यक समीकरण = C(s)+ 2H2(g) → CH4 ; ∆H = ?
समी. (ii) + समी. (iii) x 2 समी. (i) से आवश्यक समीकरण प्राप्त होगा।
∆H = -393.5 + 2 (-285.8) – (-890.3) kJ mol-1
= -74.8 kJ mol-1
सही उत्तर (a).
![]()
प्रश्न 6.
एक अभिक्रिया A + B → C+ D + q के लिए एण्ट्रॉपी परिवर्तन धनात्मक पाया गया है। यह अभिक्रिया सम्भव होगी –
(a) उच्च ताप पर,
(b) केवल निम्न ताप पर
(c) किसी भी ताप पर नहीं
(d) किसी भी ताप पर।।
उत्तर:
AG = AH – TAS, जहाँ AH = -ve, AS = +ve. अत: AG = -ve होगा सभी तापमान पर
∴ उत्तर (d).
प्रश्न 7.
एक प्रक्रम में निकाय द्वारा 701 J ऊष्मा अवशोषित होती है एवं 394 J कार्य किया जाता है। इस प्रक्रम में आन्तरिक ऊर्जा में कितना परिवर्तन होगा?
हल:
प्रश्नानुसार
q = + 701 J ( ऊष्मा अवशोषित होती है, ∴q धनात्मक है।)
W = – 394 J ( निकाय द्वारा कार्य होता है, ∴W ऋणात्मक है।)
ऊष्मागतिकी के प्रथम नियम से, आंतरिक ऊर्जा में परिवर्तन,
AU = q+ W = + 701 J + (- 394 J) = + 307 J
अतः निकाय की आंतरिक ऊर्जा में 307 J की वृद्धि होती है।
प्रश्न 8.
एक बम कैलोरीमीटर में NH2CN की अभिक्रिया डाइऑक्सीजन के साथ की गई एवं AU का मान – 742:7 kJ mol – पाया गया (298 K पर)। इस अभिक्रिया के लिए 298 K पर एन्थैल्पी परिवर्तन ज्ञात कीजिए –
NH2CN(s) + \(\frac { 3 }{ 2 }\)O2(g) → N2(g) + CO2(g) + H2O(l)
हल:
NH2CN(s) +\(\frac { 3 }{ 2 }\)O2(g) → N2(g) + CO2(g) + H2O(l)
गैसीय उत्पादों तथा अभिकारकों के मोलों की संख्या का अन्तर –
∆ng = np – nr = 2 – \(\frac { 3 }{ 2 }\) = \(\frac { 1 }{ 2 }\) = 0.5 mol
∆H = ∆U+∆ng RT
∆H = -742.7 kj mol-1 + (0.5 mol x 8:314 × 10-3kJ mol-1 × 298k)
∆H = (- 742.7 kJ + 1238.786 × 10-3kJ) mol-1
= 741-46 kJ mol-1
प्रश्न 9.
60 – 0g ऐल्युमिनियम का ताप 36°C से 55°C करने के लिए कितने किलो जूल ऊष्मा की आवश्यकता होगी ? Al की मोलर ऊष्माधारिता 24Jmol-1K-1 है।
हल:
प्रश्नानुसार,
Al का द्रव्यमान = 60.0g,
Al का मोलर द्रव्यमान = 27g mol-1,
मोलर ऊष्माधारिता,
C = 24Jmol ‘K-1,
∆T= 55°C – 35°C = 20°C या 20K.
∴ ऊष्मा, q = n – C∆T
⇒ q = \(\frac {60 }{ 27 }\) × 24Jmol-1 × 20k,
= 1066.66J = 1.067kJ.
प्रश्न 10.
10.0°C पर 1 मोल जल की बर्फ -10°C पर जमाने पर एन्थैल्पी परिवर्तन की गणना कीजिए।
∆fusH = 6.03 kJ mol-1 0°C पर,
Cp [H2O(l)] = 75.3 J mol-1K-1,
Cp[H2O(s)] = 36.8 J mol-1K-1
हल:
अभिक्रिया तीन पदों में सम्पन्न होगी:
1. जल का एक मोल 10°C पर 1 मोल जल 0°C पर परिवर्तित होगा।
∆H = n × Cp× ∆T = 1 × 75.3 (-10) = -753 J/mol-1
2. 1 मोल जल 0°C पर 1 मोल बर्फ में बदलेगा 0°C पर।
∆H = ∆गलनH × n = -6.03 kJ/mol-1 = – 6030 J/mol-1
3. 1 मोल बर्फ 0°C पर 1 मोल बर्फ में परिवर्तित होगी -10°C पर।
∆H = n × Cp× ∆T = 1 x 36.8 × (-10) = -368 J/mol-1
∴ ∆HHotel = – 753 – 6030 – 368 = – 7151 J/mol-1
![]()
प्रश्न 11.
कार्बन की कार्बन-डाइऑक्साइड में दहन की एन्थैल्पी -393.5 kJ mol-1कार्बन एवं ऑक्सीजन से 35.2gCO2 बनने पर उत्सर्जित ऊष्मा की गणना कीजिए।
हल:
C(s) + O2(g) → CO2(g);
∆H = 393.5 kJmol-1 1 mol = 44 g
∴ जब 44g CO2 बनता है तब मुक्त होने वाली ऊर्जा की मात्रा = 393.5 kJ mol-1
∴ 35.5g CO2 निर्माण होने पर मुक्त होने वाली ऊर्जा की मात्रा = \(\frac { 393.5 }{ 44 }\) × 35.2 = 314.8 kJ.
प्रश्न 12.
CO(g), CO2(g) N2O(g) एवं N2O4(g) की विरचन एन्थैल्पी क्रमशः -110, -393, 81 एवं 9.7 kJ mol-1 हैं। अभिक्रिया N2O4(g) + 3CO(g) → N2O(g)) + 3CO2(g)) के लिए ∆rH का मान ज्ञात कीजिए।
हल:
हम जानते हैं कि ∆fH° = ∑∆fH°क्रियाफल – ∑∆fH°क्रियाकारक
∆rH° = [∆fH°N2O + 3∆fH°CO2] – [∆fH°NO(2) + 3∆fH°CO2]
= [ 81 + 3 (-393)] – [9.7 + 3 (-110)] = -777.7 kJ.
प्रश्न 13.
N2(g) + 3H2(g) → 2NH3(g); ∆fH° = – 92.4kJ mol-1 NH3गैस की मानक विरचन एन्थैल्पी क्या है ?
हल:
दी गई अभिक्रिया है – N2(g) + 3H2(g) → 2NH3(g); ∆rH = -92.4kJ mol-1
∆fH°N2 = 0,
∆fH°H2 = 0,
∆fH°NH3 = x,
∆rH° = ∑∆fH°क्रियाफल – ∑∆fH° क्रियाकारक
= 2∆fH°NH3 – [∆fH°N2 + 3∆fH°H2 >]
= -92.4 = 2x
x = – \(\frac { 3 }{ 2 }\) x 92.4 = – 46.2 kJ mol-1
अर्थात् ∆fH°NH3 = – 46.2kJ mol-1
प्रश्न 14.
निम्नलिखित आँकड़ों से CH3OH(l) की मानक विरचन एन्थैल्पी ज्ञात कीजिए –
- CH3OH(l)+\(\frac { 3 }{ 2 }\) O2(g) → CO2(g)) + 2H2O(l); ∆rH° = – 726 kJ mol-1
- C(ग्रेफाइट ) + O2(g) → CO2(g)); ∆cH° = -393 kJ mol-1
- H2(g) +\(\frac { 1 }{ 2 }\)O2(g)) → H2O(l); ∆fH° = – 286 kJ mol-1
हल:
मेथेनॉल के निर्माण का आवश्यक समीकरण निम्न है –
C(s)+2H2(g) + \(\frac { 1 }{ 2 }\)O2(g) → CH3OH(l); ∆H°=?
प्रश्नानुसार, मेथेनॉल की दहन एन्थैल्पी
(i) C3OH(l)+\(\frac { 3 }{ 2 }\)O2(g)) → CO2(g)) + 2H2O(l); ∆H° = 726kJ mol-1
1 mol CO2(g) की विरचन एन्थैल्पी
(ii) C(s) + O2(g) → CO2(g); ∆H°=-393 kJ mol-1
2 mol H2O(l); के विरचन की एन्थैल्पी
(iii) H2(g) + \(\frac { 1 }{ 2 }\)O2(g) → H2O(l); ∆H° = -286kJ mol-1
समी. (iii) को 2 से गुणा करने पर,
(iv) 2H2(g) + O2(g)→ 2H2O(l) ∆H° = -572kJ mol-1
समी. (ii) तथा (iv) को जोड़ने पर,
(v) C(s) +2H2(g)+ 2O2(g) → CO2(g) + 2H2O(l); ∆H° = – 965 kJ mol-1
समी. (i) का व्युत्क्रम करने पर,
(vi) CO2(g) + 2H2O(l) → CH3OH(l) + \(\frac { 3 }{ 2 }\)O2(g)); ∆H° = 726kJ mol-1
समी. (v) तथा (vi) का योग करने पर,
C(s) + 2H2(g) + \(\frac { 1 }{ 2 }\) O2(g) → CH3OH(l); ∆H°= -239kJmol-1
![]()
प्रश्न 15.
CCI4(g) → C(g) + 4CI(g) , अभिक्रिया के लिए एन्थैल्पी परिवर्तन ज्ञात कीजिए एवं CCI4 में C – Cl की आबंध एन्थैल्पी की गणना कीजिए।
- ∆vap H°(CCl4) = 30.5 kJ mol-1
- ∆fH° (CCl4) = -135.5 kJ mol-1
- ∆aH° (C) = 715.0 kJ mol-1
- ∆aH° (Cl2) = 242 kJ mol-1 (यहाँ∆aH° कणन एन्थैल्पी है)
हल:
प्रश्नानुसार,
(i) CCI4(l)) → CCl4(g); ∆वाष्पन H° =+ 30.5kJmol-1
(ii) C(s)) + 2Cl2) → CCl4(l); ∆H°= – 135.5kJmol-1
(iii) C(s) → C(g) ; ∆H° =715.0kJmol-1
(iv) Cl2(g) → 2Cl(g); ∆,H° = 242kJ mol-1
समी. (iv) को 2 से गुणा करने पर,
(v) 2Cl2(g) → 4Cl(g); ∆H° = 484.0kJmol-1
समी. (iii) तथा (v) को जोड़ने पर,
(vi) C(s) + 2C2(g) → C(g)+ 4Cl(g); ∆H = 1199kJmol
समी. (i) तथा (ii) का व्युत्क्रम करने पर,
(vii) CCl4(g) → CCl4(l);∆H =-30.5kJmol-1
(viii) CCl4(l) → C(s) + 2Cl2(g); ∆H =+ 135.5kJmol-1
समी. (vi), (vii) तथा (viii) का योग करने पर,
CCl4(g) → C(g) + 4Cl(g) ;∆H =1304kJmol-1
CCl4 में C – Cl आबंध की आबंध एन्थैल्पी = \(\frac { 1304 }{4 }\)= 326 kJ mol-1

प्रश्न 16.
एक विलगित निकाय के लिए AU = 0, इसके लिए ∆S क्या होगा?
उत्तर:
एक विलगित तंत्र की एण्ट्रॉपी सदैव धनात्मक होती है (∆S > 0) क्योंकि ∆U = U अर्थात् ऊर्जा कारक अभिक्रिया के लिये कोई महत्व नहीं रखता है। स्वतः परिवर्तित के लिये AS को +ve होना चाहिए। उदाहरण के लिये यदि दो गैसें अलग-अलग रखी गयी हैं। तंत्र को पूर्णतः उसके परिवेश में विलगित किया गया है। मिलाने पर ∆S +ve होता है तथा तंत्र में अनियमितता ज्यादा होती है।
प्रश्न 17.
298 K पर अभिक्रिया 2A + B → C के लिए ∆H = 400 kJ mol-1 एवं ∆S = 0.2 kJK mol-1 ∆H एवं ∆S को ताप-विस्तार में स्थिर मानते हुए बताइए कि किस ताप पर अभिक्रिया स्वतः होगी?
हल:
∆H = 400 × 103 J mol-1 ;∆S = 2000 JK-1 mol-1
एक स्वतः प्रवर्तित प्रक्रम ∆G =-ve
∆H – T∆S < 0 या T >\(\frac { ∆H }{∆S }\) या T > \(\frac { 400 x 1000 }{2000 }\) या T >200K
200 K के ऊपर प्रक्रम स्वतः प्रवर्तित होगा।
प्रश्न 18.
अभिक्रिया, 2Cl(g) → Cl(g),के लिए ∆H एवं ∆S के चिन्ह क्या होंगे?
उत्तर:
(i) बंध निर्माण एक ऊष्माक्षेपी क्रिया है।
∴ ∆H = – ve
(ii) कणों की संख्या कम होने पर एण्ट्रॉपी कम होती है।
∴ ∆S = – ve
प्रश्न 19.
अभिक्रिया 2A(g) + B(g) → 2D(g) के लिए ∆U° = -10.5 kJ एवं ∆S° = – 44.1 JK-1 अभिक्रिया के लिए ∆G° की गणना कीजिए और बताइए कि क्या अभिक्रिया स्वतः प्रवर्तित हो सकती है ?
हल:
दी गयी अभिक्रिया के लिए ∆n(g) =2 – (3) = -1,
∆U° = -10.5 kJ,
R = 8:314 x 10-3 kJ,
∆T = 290 K,
∆S° = – 44.1 JK-1 = – 44.1 x 10-3kJ
∆H° = ∆U° + ∆n(g)RT
= -10.5 + (-1) (8.314 × 10-3) (290)
= -10.5 – 2.48
∆H° = -12.98 kJ
∆G° =∆H° – T∆S°
= -12.98 – 298 (-44.1 × 10-3)
= -12.98 + 13.14 = 0.16 kJ
क्योंकि ∆G° धनात्मक है अतः क्रिया स्वतः प्रवर्तित नहीं होगी।
![]()
प्रश्न 20.
300 K ताप पर एक अभिक्रिया के लिए साम्य स्थिरांक 10 है। ∆G° का मान क्या होगा ? R = 8.314 JK-1 mol-1.
हुल:
∆G° = -2.303 RT log K
= -2.303 × 8.314 × 300 × log 10
= – 5744.1 J.
प्रश्न 21.
निम्नलिखित अभिक्रियाओं के आधार पर NO(g) के ऊष्मागतिकी स्थायित्व पर टिप्पणी लिखिए –
\(\frac { 1 }{ 2 }\)N2(g) + \(\frac { 1 }{ 2 }\)O2(g) → NO(g) ; ∆fH° = 90 kJ mol-1
NO(g) + \(\frac { 1 }{ 2 }\)O2(g) → NO(g); ∆fH° = – 74 kJ mol-1
उत्तर:
NO(g),NO2की तुलना में कम स्थायी है क्योंकि NO एक ऊष्माशोषी यौगिक है जबकि NO2एक ऊष्माक्षेपी यौगिक है। ऊष्माक्षेपी यौगिक ऊष्माशोषी यौगिकों से अधिक स्थायी होती है।
प्रश्न 22.
जब 1.00 मोल H2O(l)को मानक परिस्थितियों में विरचित किया जाता है, तब परिवेश के एण्ट्रॉपी परिवर्तन की गणना कीजिए।
(∆fH° = -286 kJ mol-1)
हल:
1 mol H2O(l)) के विरचन (निर्माण) में एन्थैल्पी परिवर्तन,
H2(g) + \(\frac { 1 }{ 2 }\)O2(g)) → H2O(l);
∆fH°= -286kJ mol-1
उपर्युक्त अभिक्रिया में उत्सर्जित ऊर्जा, परिवेश द्वारा अवशोषित कर ली जाती है।
अतः
q परिवेश = + 286 kJ mol-1
![]()
= 0.9597 kJ k-1 mol-1
= 959.7 Jk-1 mol-1
ऊष्मागतिकी अन्य महत्वपूर्ण प्रश्न
ऊष्मागतिकी वस्तुनिष्ठ प्रश्न
प्रश्न 1.
सही विकल्प चुनकर लिखिए –
प्रश्न 1.
किसी तंत्र को बंद तंत्र कहा जाता है, यदि वह परिवेश के साथ विनिमय करता है –
(a) द्रव्य व ऊर्जा दोनों का
(b) द्रव्य एवं ऊर्जा में से किसी का नहीं
(c) द्रव्य का नहीं केवल ऊर्जा का
(d) ऊर्जा का नहीं केवल द्रव्य का।
उत्तर:
(c) द्रव्य का नहीं केवल ऊर्जा का
प्रश्न 2.
निम्न में से कौन-सा एन्थैल्पी परिवर्तन सदैव ऋणात्मक होता है –
(a) सम्भवन की एन्थैल्पी
(b) विलयन की एन्थैल्पी
(c) दहन की एन्थैल्पी
(d) जल अपघटन।
उत्तर:
(c) दहन की एन्थैल्पी
प्रश्न 3.
एक बम कैलोरीमीटर द्वारा निम्न का मापन होता है –
(a) ∆H
(b) ∆E
(c) qp
(d) qv.
उत्तर:
(d) qv.
प्रश्न 4.
ऊष्मागतिकी के प्रथम नियम के अनुसार.
(a) ∆ E = q + w
(b) ∆ E = q – W.
(c) ∆ E = q + PV
(d) W = ∆ E – q.
उत्तर:
(a) ∆E = q + w
प्रश्न 5.
यदि गैसीय अभिक्रिया में अभिकारकों एवं उत्पादों के मोलों की संख्या समान हो तो
(a) ∆H = ∆E
(b) ∆H > ∆E
(c) ∆H < ∆E
(d) ∆H = ∆E = 0.
उत्तर:
(a) ∆H = ∆E .
प्रश्न 6.
हेस का नियम संबंधित है –
(a) अभिक्रिया की गति से
(b) साम्य स्थिरांक से
(c) अभिक्रिया ऊष्मा में परिवर्तन से
(d) एक गैस के आयतन पर दाब के प्रभाव से।
उत्तर:
(c) अभिक्रिया ऊष्मा में परिवर्तन से
प्रश्न 7.
जब एक अम्ल की एक क्षार के साथ उदासीनीकरण ऊष्मा का मान 13.7 k cal है, तो
(a) अम्ल तथा क्षार दोनों दुर्बल होंगे
(b) अम्ल तथा क्षार दोनों प्रबल होंगे
(c) अम्ल प्रबल और क्षार दुर्बल होंगे
(d) अम्ल दुर्बल और क्षार प्रबल होंगे।
उत्तर:
(b) अम्ल तथा क्षार दोनों प्रबल होंगे.
![]()
प्रश्न 8.
अभिक्रिया CO2(g) + H2(g) → CO(g) + H2O(g) ;∆H = 80kJ , में उत्पन्न ऊष्मा को
(a) संभवन ऊष्मा कहते हैं
(b) दहन ऊष्मा कहते हैं
(c) उदासीनीकरण ऊष्मा कहते हैं
(d) अभिक्रिया ऊष्मा कहते हैं।
उत्तर:
(d) अभिक्रिया ऊष्मा कहते हैं।
प्रश्न 9.
उदासीनीकरण ऊष्मा का मान किस अभिक्रिया के लिए सबसे कम होगा –
(a) HCl + NaOH
(b) CH3COOH + NH4OH
(c) NH4OH + HCl
(d) NaOH + CH3COOH.
उत्तर:
(b) CH3COOH + NH4OH
प्रश्न 10.
अभिक्रिया C6H6(l)+ \(\frac { 15 }{ 2 }\)O2(g) → 3H2O(l), +6CO2(g)); ∆H = – 3264 kJ mol-1 है, तो 3.9 ग्राम बेन्जीन को वायु में जलाने से उत्पन्न ऊष्मा होगी –
(a) 163.23 kJ
(b) 326.4 kJ
(c) 32.64 kJ
(d) 3.264 kJ.
उत्तर:
(a) 163.23 kJ
प्रश्न 2.
रिक्त स्थानों की पूर्ति कीजिए –
- दहन ऊष्मा∆H का मान सदैव …………. होता है।
- उदासीनीकरण ऊष्मा का मान सदैव …………. kJ होता है।
- स्थिर दाब पर किसी तंत्र की सम्पूर्ण ऊष्मा को …………. कहते हैं।
- जल का वाष्पीकरण …………. परिवर्तन है।
- अभिक्रिया H2 + Cl2 → 2HCl + 44 kcal में सम्भवन ऊष्मा का मान …………. होगा।
- प्रक्रम जो तापरोधी होता है …………. कहलाता है।
- यदि उत्पादों को पूर्ण ऊष्मा अभिकारकों की पूर्ण ऊष्मा से अधिक होती है तो अभिक्रिया कहलाती है।
- नियत दाब पर ऊष्मा परिवर्तन को …………. कहते हैं।
- यदि AH का मान ऋणात्मक हो, तो अभिक्रिया …………. होती है।
- एक मोल पदार्थ को जलाने पर उत्सर्जित होने वाली ऊष्मा की मात्रा को ………… कहते हैं।
उत्तर:
- ऋणात्मक
- 57.1 kJ
- एन्थैल्पी
- ऊष्माशोषी
- 22 kcal
- रुद्धोष्म
- ऊष्माशोषी
- एन्थैल्पी
- ऊष्माक्षेपी
- दहन ऊष्मा।
![]()
प्रश्न 3.
उचित संबंध जोडिए –

उत्तर:
- (c) ऊष्माशोषी
- (d) शून्य
- (e) एन्थैल्पी
- (a) शून्य
- (b) आइसोबोरिक
प्रश्न 4.
एक शब्द / वाक्य में उत्तर दीजिए –
- अवस्था फलन के दो उदाहरण दीजिए।
- NaCl, H2O(s)) व NH3(s)) में किसकी एण्ट्रापी का मान अधिक होगा?
- ∆G = ∆H – T∆S समीकरण को किसने प्रतिपादित किया ?
- ऊष्मागतिकी के प्रथम नियम का समीकरण लिखिए।
- जब बर्फ गलकर पानी में परिवर्तित होता है तब एण्ट्रापी का मान क्या होगा?
उत्तर:
- एन्थैल्पी, एण्ट्रॉपी,
- NH3
- गिब्स हेल्महोल्ट्ज
- ∆E = q + W
- बढ़ जायेगा।
![]()
ऊष्मागतिकी अति लघु उत्तरीय प्रश्न
प्रश्न 1.
रासायनिक ऊर्जिकी शब्द का अर्थ बताइये।
उत्तर:
रासायनिक ऊर्जिकी के अंतर्गत रासायनिक अभिक्रियाओं के फलस्वरूप होने वाले ऊर्जा परिवर्तनों का अध्ययन किया जाता है।
प्रश्न 2.
298 K पर अभिक्रिया N2O4(g) ⥨ 2NO2(g) के लिए Kp का मान 0.98 है बताइए कि अभिक्रिया स्वतः प्रवर्धित होगी अथवा नहीं ?
उत्तर:
∆rG° = – 2.303 RT log Kp
Kp = 0.98 अर्थात् Kp < 1
∴ ∆G° का मान धनात्मक होगा। अतः अभिक्रिया स्वतः प्रवर्धित नहीं होगी।
प्रश्न 3.
विस्तीर्ण गुण द्रव्य की मात्रा पर निर्भर करते हैं परन्तु गहन गुण द्रव्य की मात्रा पर निर्भर नहीं करते हैं। बताइए कि निम्नलिखित गुण विस्तीर्ण है अथवा गहन गुण ? द्रव्यमान, आंतरिक ऊर्जा, दाब, ऊष्माधारिता, मोलर ऊष्माधारिता, घनत्व, मोल प्रभाज, विशिष्ट ऊष्मा, ताप तथा मोलरता।
उत्तर:
विस्तीर्ण गुण – द्रव्यमान, आंतरिक ऊर्जा, ऊष्माधारिता।
गहन गुण – दाब, मोलर ऊष्माधारिता, घनत्व, मोल प्रभाज, विशिष्ट ऊष्मा, ताप तथा मोलरता।
प्रश्न 4.
ऊष्माधारिता (Cp) एक विस्तीर्ण गुण है जबकि विशिष्ट ऊष्मा (C) एक गहन गुण है। 1 मोल जल के लिए Cr तथा C में क्या संबंध होगा?
हल:
किया गया कार्य,
W = – Pबाह्य (V2 – V1)
जब – Pबाह्य= 0,
अतः – w = – 0 (5 – 1) = 0
समतापी प्रसार के लिए, ∆U = 0
अतः ∆T = 0.
प्रश्न 5.
तंत्र किसे कहते हैं ?
उत्तर-ब्रह्माण्ड का वह विशिष्ट भाग जिसे ऊष्मागतिकी के अध्ययन के लिये चुना जाये, तंत्र या निकाय कहलाता है। यदि सम्पूर्ण निकाय के भौतिक गुण या रासायनिक संघटन समान हों तो ऐसे निकाय को समांगी निकाय कहते हैं। जैसे-गैसों का मिश्रण परन्तु यदि निकाय के सभी भागों के भौतिक गुण एवं रासायनिक संघटन भिन्न हों तो यह विषमांगी निकाय कहलाता है। उदाहरण-जल एवं तेल का मिश्रण।
![]()
प्रश्न 6.
प्रक्रम क्या है ? यह कितने प्रकार के होते हैं ?
उत्तर:
ऐसा प्रक्रम जो किसी ऊष्मागतिकी अवस्था में परिवर्तन कराता है तो उसे ऊष्मागतिकी प्रक्रम कहते हैं।
ऊष्मागतिकी प्रक्रम के प्रकार –
- समतापी प्रक्रम
- रुद्धोष्म प्रक्रम
- समदाबी प्रक्रम
- समआयतनिक प्रक्रम
- उत्क्रमणीय प्रक्रम
- अनुत्क्रमणीय प्रक्रम
- चक्रीय प्रक्रम।
प्रश्न 7.
ऊष्माक्षेपी अभिक्रिया किसे कहते हैं ? उदाहरण सहित समझाइये। अथवा, ऊष्माक्षेपी अभिक्रिया के लिये ∆H का चिह्न ऋणात्मक होता है, क्यों?
उत्तर:
ऐसी अभिक्रियाएँ जिनमें अभिक्रिया के दौरान ऊष्मा उत्सर्जित होती है, ऊष्माक्षेपी अभिक्रियाएँ कहलाती हैं। ऐसी अभिक्रियाओं में अभिकारकों की एन्थैल्पी उत्पादों की एन्थैल्पी से अधिक होती है। इसलिये अभिक्रिया के दौरान ऊष्मा का उत्सर्जन होता है, अत: ऐसी अभिक्रियाओं हेतु एन्थैल्पी का मान ऋणात्मक होता है।
2NO(g) → N2(g) + O2(g) ; ∆H = -180.5kJ/mol-1
प्रश्न 8.
विस्तीर्ण एवं गहन गुण को उदाहरण सहित समझाइये।
उत्तर:
1. विस्तीर्ण गुण-निकाय के वे गुण जो पदार्थ की मात्रा पर निर्भर करते हैं, विस्तीर्ण गुण या मात्रात्मक गुण कहलाते हैं।
उदाहरण-द्रव्यमान, आयतन, ऊष्माधारिता।
2. गहन गुण-निकाय के वे गुण जो पदार्थ की मात्रा पर निर्भर नहीं करते हैं, गहन गुण या विशिष्ट गुण कहलाते हैं।
उदाहरण-ताप, दाब, पृष्ठ तनाव, श्यानता।
प्रश्न 9.
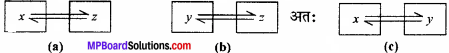
ऊष्मागतिकी का शून्य नियम किसे कहा जाता है ?
उत्तर:
इस नियम को तापीय साम्य का नियम भी कहा जाता है। इस नियम के अनुसार-“दो पिण्ड यदि अलग-अलग किसी तीसरे पिण्ड के तापीय साम्य में हैं तो आपस में भी एक-दूसरे के तापीय साम्य में होंगे।”
प्रश्न 10.
उदासीनीकरण ऊष्मा को परिभाषित कीजिए।
उत्तर:
उदासीनीकरण ऊष्मा निकाय की एन्थैल्पी में वह परिवर्तन है जो किसी अम्ल का एक ग्राम तुल्यांक तनु विलयन में किसी क्षार के एक ग्राम तुल्यांक द्वारा पूर्णतः उदासीन करने पर होता है।
HClaq+ NaOHaq ⥨ NaClaq+ H2O(l); ∆H = -57.1 kJ
![]()
प्रश्न 11.
दुर्बल अम्ल एवं प्रबल क्षार की उदासीनीकरण ऊष्मा का मान प्रबल अम्ल व प्रबल क्षार की उदासीनीकरण ऊष्मा के मान से कम होता है, क्यों?
उत्तर:
दुर्बल अम्ल एवं प्रबल क्षार की उदासीनीकरण ऊष्मा का मान कम होता है क्योंकि निकलने वाली ऊष्मा का कुछ भाग दुर्बल अम्ल या क्षार का पूर्ण वियोजन करने में खर्च हो जाती है। अतः परिणामस्वरूप दुर्बल अम्ल एवं क्षार का प्रबल क्षार या प्रबल अम्ल द्वारा उदासीनीकरण करने पर प्राप्त ऊष्मा का मान प्रबल अम्ल एवं प्रबल क्षार के उदासीनीकरण से प्राप्त ऊर्जा के मान से कम प्राप्त होता है।
![]()
प्रश्न 12.
आबन्ध वियोजन ऊर्जा या बंध एन्थैल्पी किसे कहते हैं ?
उत्तर:
किसी रासायनिक बंध के बनते समय ऊर्जा मुक्त होती है। अत: बंध को तोड़ने हेतु भी ऊर्जा की आवश्यकता होती है। किसी बंध को तोड़ने हेतु आवश्यक ऊर्जा बंध, एन्थैल्पी कहलाती है। अत: वह एन्थैल्पी परिवर्तन है जो गैसीय अणु को परमाणुओं में तोड़ने के लिये आवश्यक है।
HCl(g) → H(g) + Cl(g) ; ∆H = 431kJ/mol-1
प्रश्न 13.
ऊष्मागतिकी का प्रथम नियम क्या है ?
उत्तर:
ऊष्मागतिकी के प्रथम नियम को ऊर्जा का संरक्षण नियम भी कहा जाता है। इसके अनुसार, “ऊर्जा को न तो उत्पन्न किया जा सकता है और न ही नष्ट किया जा सकता है, इसे केवल एक रूप से दूसरे रूप में परिवर्तित किया जा सकता है।” माना कि तंत्र की आंतरिक ऊर्जा U1 है, यदि इस तंत्र को व ऊष्मा दी जाये तो तंत्र की आंतरिक ऊर्जा बढ़कर U1 + q हो जायेगी। यदि किया गया कार्य w है तो आंतरिक ऊर्जा बढ़कर U2 के बराबर हो जाती है।
अतः U2 – U1 =q + W
या ∆U = q + W.
प्रश्न 14.
एण्ट्रॉपी को परिभाषित कीजिये।
उत्तर:
एण्ट्रॉपी किसी निकाय की अव्यवस्था या यादृच्छिकता की माप है। कोई निकाय जितना अधिक अव्यवस्थित होगा, उसकी एण्ट्रॉपी का मान उतना ही अधिक होगा। किसी पदार्थ की क्रिस्टलीय ठोस अवस्था में एण्ट्रॉपी का मान न्यूनतम तथा गैसीय अवस्था में एण्ट्रॉपी का मान अधिकतम होता है।
प्रश्न 15.
जल वाष्प, जल तथा बर्फ में किसकी एण्ट्रॉपी अधिक है और क्यों ?
उत्तर:
एण्ट्रॉपी अनियमितता का मापक होती है। ठोस अवस्था में अणु पूर्ण रूप से व्यवस्थित होते हैं, इसलिये इसकी एण्ट्रॉपी न्यूनतम होती है तथा गैस में अणु सभी दिशाओं में अनियमित रूप से गति करते रहते हैं इसलिये एण्ट्रॉपी का मान अधिकतम होता है। अतः
S(बर्फ) < S(जल)) < S(जल वाष्प)
प्रश्न 16.
NaCl, H2O तथा NH3 में किसकी एण्ट्रॉपी अधिकतम होगी और क्यों?
उत्तर:
एण्ट्रॉपी अनियमितता की माप होती है। ठोस अवस्था में अणु पूर्ण रूप से व्यवस्थित होते हैं, इसलिये इसकी एण्ट्रॉपी न्यूनतम होती है। जबकि गैस में अणु सभी दिशाओं में अनियमित गति करते हैं, इसलिये इसकी एण्ट्रॉपी अधिकतम होती है। उपर्युक्त उदाहरण में NaCI ठोस, H2O द्रव तथा NH3गैस है इसलिये NH3 की एण्ट्रॉपी सबसे अधिक तथा NaCl की एण्ट्रॉपी सबसे कम होती है।
![]()
प्रश्न 17.
सिद्ध कीजिए – P∆V = ∆nRT.
उत्तर:
आदर्श गैस समीकरण से,
PV = nRT
यदि प्रारम्भिक अवस्था में गैस का आयतन V1 तथा गैस के मोलों की संख्या n हो तो
PV1 = n1 RT
यदि अंतिम अवस्था में गैस का आयतन V2 तथा गैस के मोलों की संख्या n2 हो तो
PV2 =n2RT
समी. (1) और (2) से,
P(V2 – V1) =(n2 – n1)RT
या P∆V = ∆nRT.
प्रश्न 18.
∆H तथा ∆U में क्या संबंध है ?
उत्तर:
यदि किसी तंत्र की एन्थैल्पी H तथा आंतरिक ऊर्जा U है तो एन्थैल्पी तथा आन्तरिक ऊर्जा में निम्नलिखित संबंध है –
H = U + PV
एन्थैल्पी परिवर्तन हेतु, ∆H = ∆U + P∆V
हम जानते हैं, P∆V = ∆nRT
मान रखने पर, ∆H = ∆U + ∆nRT
प्रश्न 19.
विशिष्ट ऊष्माधारिता से क्या अभिप्राय है ?
उत्तर:
एक ग्राम पदार्थ का ताप 1 डिग्री वृद्धि हेतु आवश्यक ऊष्मा विशिष्ट ऊष्मा कहलाती है। इसे Cs से दर्शाते हैं।
Cs= \(\frac { C }{ M }\)
जहाँ C = ऊष्माधारिता, Cs = विशिष्ट ऊष्माधारिता, m = पदार्थ का द्रव्यमान। इसकी S.I. इकाई जूल प्रति केल्विन प्रति ग्राम है।
प्रश्न 20.
मोलर ऊष्माधारिता से क्या समझते हैं ?
उत्तर:
किसी पदार्थ के एक मोल का ताप एक डिग्री बढ़ाने हेतु आवश्यक ऊष्मा की मात्रा मोलर ऊष्माधारिता कहलाती है।
मोलर ऊष्माधारिता = \(\frac { C }{∆T×m }\)
जहाँ C = अवशोषित ऊष्मा, ∆T = ताप में वृद्धि, m = आण्विक द्रव्यमान। इसकी SI इकाई जूल प्रति केल्विन प्रति मोल है।
प्रश्न 21.
हेस का नियम लिखिए।
उत्तर:
हेस ने इस नियम का प्रतिपादन सन् 1840 में किया था। इस नियम के अनुसार, “यदि कोई रासायनिक परिवर्तन दो या दो से अधिक विधियों द्वारा या एक या एक से अधिक पदों में किया जाये तो संपूर्ण परिवर्तन में उत्पन्न अथवा अवशोषित ऊष्मा की मात्रा स्थिर रहती है, चाहे वह परिवर्तन किसी भी विधि द्वारा किया गया हो”
![]()
प्रश्न 22.
रुद्धोष्म प्रक्रम क्या है ?
उत्तर:
जब कोई प्रक्रम इस प्रकार कराया जाता है कि निकाय तथा घिराव के बीच किसी प्रकार से ऊष्मा का विनिमय संभव नहीं होता तो इस प्रकार के प्रक्रम को रुद्धोष्म प्रक्रम कहते हैं। इस प्रकार के प्रक्रम प्रायः विलगित निकाय में होते हैं। इस प्रकार के प्रक्रम के लिये dq = 0 होता है।
प्रश्न 23.
मानक संभवन एन्थैल्पी क्या है ?
उत्तर:
मानक अवस्था में अर्थात् 298 K ताप (25°C) और 1 वायुमण्डलीय दाब (760 mm) पर किसी उत्पाद के 1 मोल को उसके अवयवी तत्वों से बनाने में जो एन्थैल्पी परिवर्तन होता है, उसे मानक संभवन की एन्थैल्पी कहते हैं। इसे ∆H°f या ∆f H° से दर्शाते हैं।
प्रश्न 24.
विलयन की एन्थैल्पी क्या है ? उदाहरण सहित समझाइये।
उत्तर:
किसी पदार्थ के 1 मोल को विलायक के आधिक्य में पूरी तरह घोलने पर होने वाला ऊष्मा परिवर्तन विलयन की एन्थैल्पी कहलाती है। विलायक के आधिक्य का तात्पर्य यह है कि विलयन बनने के बाद इसमें विलायक की मात्रा मिलाने पर किसी प्रकार का ऊष्मा परिवर्तन न हो। उदाहरण – KCl(s) + aq → KCl(aq); ∆H = + 18.6kJ
प्रश्न 25.
जलयोजन की एन्थैल्पी क्या है ? उदाहरण सहित समझाइये।
उत्तर:
जब किसी निर्जलीय लवण का एक मोल जल के कुछ निश्चित संख्या में अणुओं से संयुक्त होकर जलीय लवण बनाता है तो अभिक्रिया में होने वाला ऊष्मा परिवर्तन जलयोजन की एन्थैल्पी कहलाती है। उदाहरण – CuSO4(s) + 5H2O(l) → CuSO4.5H2O; ∆H = -78.2 kJ
प्रश्न 26.
गलन की एन्थैल्पी क्या है ? उदाहरण सहित समझाइये।
उत्तर:
गलन की एन्थैल्पी (Heat of fusion):
एक मोल ठोस को उसके गलनांक तथा 1 वायुमण्डलीय दाब पर 1 मोल द्रव में परिवर्तित करने पर होने वाले एन्थैल्पी परिवर्तन को ठोस की गलन ऊष्मा या गलन की एन्थैल्पी कहते हैं। उदाहरण-बर्फ के गलनांक पर 1 मोल बर्फ को 1 मोल जल में परिवर्तित करने के लिए 601 kJ ऊर्जा लगती है।
H2O2 → H2O(l); ∆H = + 6.01kJ
अत: 273 K पर बर्फ की गलन की एन्थैल्पी (ऊष्मा) = 6.01 kJ.
![]()
प्रश्न 27.
एक विलगित निकाय के ∆U = 0, इसके लिए ∆S क्या होगा?
उत्तर:
किसी विलगित निकाय के लिए, ∆U = 0 तथा किसी सतत् प्रक्रम के लिए, एन्ट्रॉपी में कुल परिवर्तन धनात्मक होना चाहिए। उदाहरण के लिए, किसी बंद पात्र, जो कि परिवेश से विलगित है, में दो गैसों A तथा B को विसरित करते हैं। दोनों गैसों A तथा B को एक गतिक विभाजक से पृथक् किया गया है। जब विभाजक हटाया जाता है, तो गैसें आपस में विसरित होने लगती हैं तथा निकाय अधिक अव्यवस्थित हो जाता है। इस प्रक्रम के लिए, ∆S > 0 तथा ∆U = 0.
![]()
अतः T∆S अथवा ∆S > 0.
ऊष्मागतिकी लघु उत्तरीय प्रश्न
प्रश्न 1.
ऊर्जा संरक्षण नियम क्या है? इसका गणितीय व्यंजक भी लिखिए। अथवा, ऊष्मागतिकी का प्रथम नियम क्या है? इसका गणितीय व्यंजक प्रतिपादित कीजिए।
उत्तर:
ऊष्मागतिकी का प्रथम नियम ऊर्जा संरक्षण का नियम है, इस नियम के अनुसार, “ऊर्जा को न तो उत्पन्न किया जा सकता है और न ही नष्ट किया जा सकता है, इसे केवल एक रूप से दूसरे रूप में परिवर्तित किया जा सकता है।” दूसरे शब्दों में, “जब कभी ऊर्जा की कोई निश्चित मात्रा एक रूप में अदृश्य या विलुप्त होती है तो ऊर्जा की तुल्य मात्रा दूसरे रूप में प्रकट हो जाती है।”
गणितीय व्यंजक:
माना किसी निकाय की आंतरिक ऊर्जा U1 है तथा यह परिपार्श्व से q ऊष्मा ऊर्जा अवशोषित करता है अतः इसकी आंतरिक ऊर्जा बढ़कर U1 + q हो जायेगी। यदि निकाय पर W कार्य किया जाता है तो आंतरिक ऊर्जा बढ़कर U1 + q + W हो जायेगी तथा यह U2 के बराबर है।
U2 = U1 + q + W.
या U2 – U1 = q+ W
या ∆U =q + w, (∴ U2 – U1 = ∆U)
प्रश्न 2.
ऊष्मागतिकी के प्रथम नियम को कभी ∆E = q – W से दर्शाया जाता है तथा कभीकभी ∆E = q + w से दर्शाया जाता है। क्यों ?
उत्तर:
यदि तंत्र द्वारा घिराव पर कार्य होता है तो तंत्र की कुछ ऊर्जा कार्य करने में प्रयुक्त होती है जिसके कारण तंत्र की आंतरिक ऊर्जा में कमी आती है तथा तंत्र द्वारा किया गया कार्य ऋणात्मक होता है। इस परिस्थिति में ऊष्मागतिकी के प्रथम नियम को ∆E =q – W से दर्शाया जाता है। दूसरी तरफ यदि तंत्र पर घिराव द्वारा कार्य होता है तो किया गया कार्य धनात्मक होता है क्योंकि तंत्र की आंतरिक ऊर्जा में वृद्धि होती है और इस स्थिति में ऊष्मागतिकी के प्रथम नियम को ∆E = q + W द्वारा दर्शाया जाता है।
प्रश्न 3.
उत्क्रमणीय प्रक्रम तथा अनुत्क्रमणीय प्रक्रम में अंतर स्पष्ट कीजिए।
उत्तर:
उत्क्रमणीय प्रक्रम तथा अनुत्क्रमणीय प्रक्रम में अंतर –
उत्क्रमणीय प्रक्रम:
- ये प्रक्रम अत्यन्त धीमी गति से संचालित होता हैं। इसमें संचालनकारी एवं विपरीतकारी बल व विपरीतकारी बलों के बीच अंतर अत्यन्त सूक्ष्म होता है।
- ये अधिकांशतः सैद्धान्तिक प्रक्रम होते हैं।
- इन प्रक्रमों को पूर्ण होने में अधिक समय लगता है।
- इन प्रक्रमों में किया गया कार्य अधिकतम होता है।
- प्रक्रम के दौरान किसी भी समय साम्यावस्था नष्ट नहीं होती है।
अनुत्क्रमणीय प्रक्रम:
- ये प्रक्रम तेजी से घटित होते हैं। इनमें संचालनकारी बल में काफी अंतर होता है।
- ये अधिकांशतः वास्तविक व स्वतः प्रवर्तित होते है।
- इनको पूर्ण होने में निश्चित समय लगता है।
- इन प्रक्रमों में किया गया कार्य अधिकतम नहीं होता है।
- प्रक्रिया पूर्ण होने के पश्चात् ही साम्यावस्था प्राप्त हो जाती है।
![]()
प्रश्न 4.
निम्नलिखित अभिक्रियाओं के आधार पर NO(g) के ऊष्मागतिकीय स्थायित्व पर टिप्पणी कीजिए –
\(\frac { 1 }{ 2 }\)N2(g) + \(\frac { 1 }{ 2 }\)O2(g) → NO2(g) ; ∆H° = 90kJ mol-1
NO(g) + \(\frac { 1 }{ 2 }\)O2(g) → NO2(g); ∆H° = 74kJmol-1
उत्तर:
NO(g) अस्थायी है, क्योंकि NO का निर्माण एक ऊष्माशोषी प्रक्रम है (अर्थात् ऊष्मा अवशोषित होती है) परन्तु NO2(g) का निर्माण होता है (स्थायी) क्योंकि इसका निर्माण ऊष्माक्षेपी प्रक्रम है (अर्थात् ऊष्मा उत्सर्जित होती है)। अतः अस्थायी NO(g)स्थायी NO2(g) में परिवर्तित हो जाता है।
प्रश्न 5.
साम्यावस्था पर ∆rG तथा ∆rG° में से कौन-सी राशि का मान शून्य होगा?
उत्तर:
∆rG = ∆rG° + RTInK
साम्यावस्था पर, 0 = ∆G° + RTInK
अथवा ∆rG° = – RTInK
∆rG° = 0
K के अन्य समस्त मानों के लिए ∆rG° के मान अशून्य होंगे।
प्रश्न 6.
स्थिर आयतन पर किसी विलगित निकाय की आन्तरिक ऊर्जा में परिवर्तन ज्ञात कीजिए।
उत्तर:
किसी विलगित निकाय की ऊर्जा का ऊष्मा अथवा कार्य के रूप में स्थानान्तरण नहीं होता है। अतः ऊष्मागतिकी के प्रथम नियम से –
∆U =q + W = 0 + 0 = 0.
प्रश्न 7.
ऊष्माधारिता क्या है ? Cp– Cv = R व्यंजक को स्थापित कीजिये।
उत्तर:
ऊष्माधारिता-किसी निकाय का ताप 1°C बढ़ाने के लिये आवश्यक ऊष्मा की मात्रा को ऊष्माधारिता कहा जाता है। इसकी इकाई जूल प्रति केल्विन है।
Cpएवं Cv में संबंध –
स्थिर आयतन पर ऊष्माधारिता,
Cv = \(\frac { ∆V }{ ∆T }\)v
∆V = Cv∆T = qv
इसी प्रकार स्थिर दाब पर ऊष्माधारिता,
Cp = \(\frac { ∆H }{ ∆T }\)p
∆V = Cp∆T = qp
आदर्श गैस के 1 मोल हेतु,
∆H = ∆V + ∆(PV)
∆H = ∆V + ∆(RT),(∴ PV = RT)
∆H = AV + R∆T
मान रखने पर, Cp∆T = Cv∆T+R∆T
∆T से भाग देने पर,
Cp = CV+R
Cp – CV = R
![]()
प्रश्न 8.
दहन ऊष्मा को समझाइये। इसके उपयोग भी लिखिए।
उत्तर:
दहन ऊष्मा-निश्चित ताप व स्थिर दाब पर किसी यौगिक के 1 मोल की ऑक्सीजन के आधिक्य में पूर्ण दहन करने पर जो ऊर्जा का परिवर्तन होता है, उसे उस यौगिक की दहन ऊष्मा कहते हैं।
उदाहरण – CH4 + 2O2→ CO2 + 2H2O; ∆H = -212kcal
C(s) + O2(g) → CO2(g); ∆H = -94.3kcal
इन अभिक्रियाओं में क्रमश: मेथेन के एक अणु व कार्बन के एक अणु का ऑक्सीजन के साथ पूर्ण दहन होता है। इन अभिक्रियाओं की एन्थैल्पी को दहन की एन्थैल्पी भी कहते हैं। दहन ऊष्मा हमेशा उत्सर्जित होती है।
दहन ऊष्मा के उपयोग:
- ईंधन का ऊष्मीय मान या कैलोरी मान ज्ञात करने में।
- यौगिकों की सम्भवन ऊष्मा निर्धारण में।
- यौगिकों की संरचना निर्धारण में।
- भोजन के कैलोरी मूल्य के परिकलन में।
प्रश्न 9.
निर्वात् में किसी गैस का प्रसार, मुक्त प्रसार कहलाताहै। यदि किसी आदर्श गैस के IL समतापीय विस्तार द्वारा 5L तक प्रसारित हो जाते हैं, तो किया गया कार्य तथा आन्तरिक ऊर्जा में परिवर्तन ज्ञात कीजिए।
हल:
किया गया कार्य, W = – Pबाह्य (V2 – V1)
Pबाह्य = 0,
अतः W= – 0 (5 – 1) = 0
समतापी प्रसार के लिए, ∆U = 0
अतः ∆T = 0
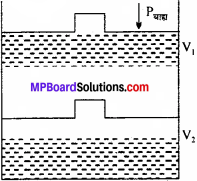
प्रश्न 10.
किसी सिलेण्डर में बंद आदर्श गैस को चित्रानुसार एकल पद में नियत बाह्य दाब, Pबाह्य द्वारा संपीडित किया जाता है, तो गैस पर किया गया कार्य कितना होगा ? ग्राफ द्वारा समझाइए।
हल:
माना प्रारम्भ में गैस का कुल आयतन Vi तथा सिलेण्डर गैस का दाब P है। एकल पद में बाह्य दाब Pबाह्य द्वारा संपीडित करने पर गैस का अन्तिम आयतन Vf हो जाता है।
अतः आयतन में परिवर्तन, ∆V = (Vf – Vi)
यदि पिस्टन की गति के कारण निकाय पर W कार्य हो, तब। किया गया कार्य,
w = Pबाह्य (-∆V)
w = Pबाह्य (Vf – Vi)
इसे चित्र में अंकित P – V ग्राफ द्वारा ज्ञात कर सकते हैं। किया गया कार्य छायांकित भाग ABVfVi, के बराबर होता है। कार्य का ऋणात्मक मान दर्शाता है कि कार्य निकाय पर किया गया है।
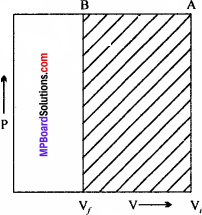
प्रश्न 11.
वाष्पन की ऊष्मा एवं सम्भवन की ऊष्मा को परिभाषित कीजिये।
उत्तर:
वाष्पन की ऊष्मा-द्रव से वाष्प तथा वाष्प से द्रव में परिवर्तन से एन्थैल्पी में होने वाले परिवर्तन को वाष्पन की एन्थैल्पी कहते हैं, या एक मोल द्रव को उसके क्वथनांक तथा एक वायुमण्डलीय दाब पर वाष्प में परिवर्तित करने पर होने वाले एन्थैल्पी परिवर्तन को द्रव की वाष्पीकरण ऊष्मा या वाष्पन की एन्थैल्पी कहते हैं।
उदाहरण – H2O(l) ⥨ H2O(g) ); ∆H = + 40.7kJ
संभवन ऊष्मा:
एक निश्चित ताप व स्थिर दाब पर किसी यौगिक के एक मोल उत्पाद को उसके अवयवी तत्वों से बनाने में जो एन्थैल्पी परिवर्तन होता है, उसे संभवन की एन्थैल्पी या संभवन की ऊष्मा कहते हैं। इसे ∆Hf से दर्शाते हैं।
C(s) + O2(g) → CO2(g); ∆H = -393.5kJ/mol
![]()
प्रश्न 12.
संलयन की एन्थैल्पी तथा ऊर्ध्वपातन की एन्थैल्पी को उदाहरण सहित समझाइये।
उत्तर:
संलयन की एन्थैल्पी-एक मोल ठोस को उसके गलनांक तथा एक वायुमण्डलीय दाब पर एक मोल द्रव में परिवर्तित करने पर होने वाला एन्थैल्पी परिवर्तन ठोस की गलन ऊष्मा या संलयन की एन्थैल्पी कहलाता है।
H2O(s) ⥨ H2O(l); ∆H = + 6.01kJ
ऊर्ध्वपातन की एन्थैल्पी:
जब एक मोल ठोस अपने गलनांक से कम ताप पर बिना द्रव अवस्था में परिवर्तित हुए सीधे गैस अवस्था में परिवर्तित हो जाता है, तो इस प्रक्रिया में एन्थैल्पी का परिवर्तन, ऊर्ध्वपातन की एन्थैल्पी कहलाता है।
I(s) ⥨ I2(g); ∆H = + 62 . 4kJ
प्रश्न 13.
वाष्पीकरण प्रक्रम में एण्ट्रॉपी में किस प्रकार परिवर्तन होता है ?
उत्तर:
वाष्पीकरण की एण्ट्रॉपी-एक मोल द्रव को उसके क्वथनांक तथा एक वायुमण्डलीय दाब पर वाष्प अवस्था में परिवर्तित करने पर जो एण्ट्रॉपी परिवर्तन होता है, उसे वाष्पीकरण की एण्ट्रॉपी कहते हैं। मान लो स्थिर दाब पर एक मोल द्रव अपने क्वथनांक Tb पर द्रव अवस्था से वाष्प अवस्था में उत्क्रमणीय रूप से परिवर्तित होता है। यदि इस पदार्थ की मोलर वाष्पन ऊष्मा ∆Hवाष्पन हो तो वाष्पन प्रक्रम में एण्ट्रॉपी परिवर्तन ∆Sवाष्पन को निम्न प्रकार से व्यक्त किया जा सकता है –
![]()
चूँकि∆Hगलनतथा ∆Hवाष्पनदोनों धनात्मक होते हैं। अतः गलन तथा वाष्पन दोनों प्रक्रम में एण्ट्रॉपी में वृद्धि होती है।
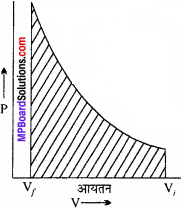
प्रश्न 14.
आप किसी आदर्श गैस के संपीडन में किए गए कार्य की गणना किस प्रकार करेंगे जबकि दाब में परिवर्तन अनन्त पदों में किया गया हो?
उत्तर:
जब दाब में परिवर्तन अनन्त पदों में किया गया हो, तो यह एक उत्क्रमणीय प्रक्रम होता है। अत: गैस पर किया गया कार्य छायांकित भाग में दर्शाया गया है।
प्रश्न 15.
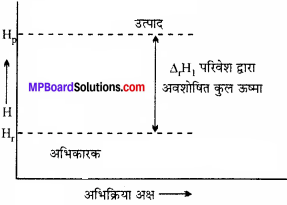
किसी अभिक्रिया के लिए एन्थैल्पी आरेख संलग्न चित्र में दर्शाया गया है। क्या दिए गए चित्र द्वारा दी गई अभिक्रिया की सततता का निश्चय करना सम्भव है?
उत्तर:
नहीं, एन्थैल्पी किसी अभिक्रिया की द्वारा सततता का विनिश्चय करने वाले कारकों में से एक कारक है, परन्तु यह अकेला कारक नहीं है। इसके लिए अन्य कारकों जैसे – ∆G, ∆S, T के साथ-साथ एन्ट्रॉपी ∆S पर भी विचार किया जाता है।
प्रश्न 16.
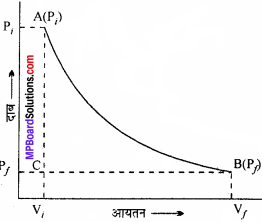
किसी आदर्श गैस की उत्क्रमणीय अभिक्रिया अक्षतथा समतापी प्रक्रम द्वारा (PiVi) से (PfVf) में। अवस्था परिवर्तन होती है। इस प्रसार में किए गए कार्य को ग्राफीय रूप में प्रदर्शित कीजिए। PV ग्राफ की। सहायता से, स्थिर बाह्य दाब Pf के विरुद्ध किए गए कार्य की उपरोक्त कार्य से तुलना कीजिए।
उत्तर:
(i) उत्क्रमणीय कार्य कुल क्षेत्र ABC तथा . BCViVfद्वारा प्रदर्शित है।
(ii) स्थिर दाब P के परितः किया गया कार्य क्षेत्र PfBCViVf द्वारा प्रदर्शित है।
अतः कार्य (i) > कार्य (ii)।
प्रश्न 17.
आन्तरिक ऊर्जा से क्या तात्पर्य है ? क्या इसका वास्तविक मान प्राप्त किया जा सकता है ?
उत्तर:
प्रत्येक पदार्थ के अंदर ऊर्जा की कुछ मात्रा निहित रहती है जो उस पदार्थ की रासायनिक प्रकृति, ताप, दाब व आयतन तथा भौतिक अवस्था पर निर्भर करती है। इसे आंतरिक ऊर्जा कहते हैं तथा U से दर्शाते हैं। आंतरिक ऊर्जा विभिन्न प्रकार की गतिज ऊर्जा तथा स्थितिज ऊर्जा का योग होती है। जैसे- घूर्णन ऊर्जा (Er), कम्पन ऊर्जा (Ev), स्थानांतरण ऊर्जा (Et), इलेक्ट्रॉनिक ऊर्जा (Ee), नाभिकीय ऊर्जा (En), और अणुओं के बीच उपस्थित आकर्षण बल के कारण उत्पन्न ऊर्जा Ei
अतः U = E e+ En+Et+Er+ Ev+Ei आंतरिक ऊर्जा की अवयवी ऊर्जा जैसे-कम्पन ऊर्जा, घूर्णन ऊर्जा के मान सही-सही प्राप्त नहीं किये जा सकते। अतः पदार्थ की आन्तरिक ऊर्जा के निरपेक्ष मान का सही-सही निर्धारण संभव नहीं है।
![]()
प्रश्न 18.
अभिक्रिया की एन्थैल्पी को प्रभावित करने वाले कारक क्या हैं ?
उत्तर:
किसी अभिक्रिया की एन्थैल्पी निम्न कारकों पर निर्भर करती है –
(1) अभिकारकों व उत्पाद की भौतिक अवस्था:
अभिकारकों व उत्पाद की भौतिक अवस्था एन्थैल्पी को प्रभावित करती है क्योंकि इसमें गुप्त ऊष्मा भी सम्मिलित होती है।
H2(g) + \(\frac { 1 }{ 2 }\)O2(g)→ H2O(l)); ∆H = -286kJ
H2(g) + \(\frac { 1 }{ 2 }\)O2(g)→ H2O(g)); ∆H = -249kJ
(2) अभिकारक की मात्रा:
अभिकारकों की मात्रा पर भी अभिक्रिया की एन्थैल्पी निर्भर करती है। जैसे – 1 मोल H2 के[ latex]\frac { 1 }{ 2 }[/latex] मोल O2 से अभिक्रिया करने पर 286 kJ ऊष्मा उत्पन्न होती है। 2 मोल में यह मात्रा दो गुनी हो जाती है।
H2(g) + \(\frac { 1 }{ 2 }\) O2(g) → H2O(l); ∆H = – 286kJ
2H2(g) + O2(g) → 2H2O(l); ∆H = -572kJ
(3) अभिकारकों का अपरूपीय रूपान्तरण-एक ही पदार्थ के भिन्न-भिन्न अपरूपों के लिये एन्थैल्पी परिवर्तन अलग-अलग होगा।
Cप्रेफाइट + O2(g) → CO2(g); ∆H = -393.5kJ
Cहीरा + O2(g) → CO2(g); ∆H = -395.4kJ
(4) ताप – अभिक्रिया की एन्थैल्पी ताप पर निर्भर करती है।
25°C पर – H2(g)+ Cl2(g) → 2HCl(g); ∆H = -184.4kJ
75°C पर – H2(g)+ Cl2(g) → 2HCl2(g); ∆H = +184.4kJ
प्रश्न 19.
सिद्ध कीजिए कि स्थिर आयतन पर qv = ∆U.
उत्तर:
जब कोई क्रिया स्थिर आयतन पर करायी जाती है तो तंत्र द्वारा कोई कार्य नहीं होता। अतः W=0.
अतः ∆U =q+w
मान रखने पर, ∆U =q
अतः स्थिर आयतन पर जो ऊष्मा अवशोषित होती है वह तंत्र की आन्तरिक ऊर्जा में वृद्धि करने के ही काम आती है।
अतः ∆U =q + W =q + P∆V, (W = P∆V) चूँकि क्रिया स्थिर आयतन पर हो रही है इसलिये ∆V = 0 होगा।
मान रखने पर, ∆Uv =qp
प्रश्न 20.
हेस का स्थिर ऊष्मा संकलन नियम के अनुप्रयोग लिखिए।
उत्तर:
हेस का स्थिर ऊष्मा संकलन नियम के अनुप्रयोग निम्नलिखित हैं –
- संभवन की एन्थैल्पी का निर्धारण करने में।
- अपरूपीय संक्रमणों की एन्थैल्पी का निर्धारण करने में।
- जलयोजन के एन्थैल्पी की गणना करने में।
- किसी अभिक्रिया के लिये एन्थैल्पी परिवर्तन ज्ञात करने में।
- बंध ऊर्जा के निर्धारण में।
- दहन की एन्थैल्पी का निर्धारण करने में।
प्रश्न 21.
किसी ईंधन के कैलोरी मान का क्या अभिप्राय है ? उदाहरण सहित समझाइये।
उत्तर:
एक ग्राम भोजन या ईंधन के दहन से कैलोरी या जूल के रूप में उत्पन्न ऊष्मा को भोजन या ईंधन का कैलोरी मान कहते हैं।
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(g) ; ∆H = -2840kJ
इस अभिक्रिया में 1 मोल ग्लूकोज अर्थात् 180 ग्राम से प्राप्त ऊष्मा = 2840kJ
अतः 1 ग्राम ग्लूकोज से प्राप्त ऊष्मा = \(\frac { 2840 }{ 180 }\) = 15. 78kJ/gm
अतः ग्लूकोज का कैलोरी मान 15.78 kJ/gm है।
ऊष्मागतिकी दीर्घ उत्तरीय प्रश्न
प्रश्न 1.
सिद्ध कीजिए –
∆H = ∆U+P∆V. अथवा, ∆H तथा ∆U में संबंध समझाइए।
उत्तर:
ऊष्मागतिकी के प्रथम नियमानुसार,
q = ∆U+w,
q = ∆U+ P∆V, (W = P∆V) ……..(1)
एन्थैल्पी के अनुसार,
q= AH ……..(2)
समी, (1) और (2) से,
∆H= ∆U + P∆V ……..(3)
आदर्श गैस समीकरण से,
PV = nRT
माना प्रारम्भिक स्थिति में गैस का आयतन V1तथा गैस के मोलों की संख्या n है, तो
PV1 = n1 RT ……..(4)
माना अंतिम स्थिति में गैस का आयतन V2तथा गैस के मोलों की संख्या n2 है, तो
PV2= n2RT ……..(5)
समी. (5) में से समी. (4) को घटाने पर,
P(V2 – V1) = (n2 – n1) RT या P∆V=∆nRT
समी. (3) में मान रखने पर,
∆H = ∆U + ∆nRT
परिस्थिति:
(1) यदि उत्पाद के मोलों की संख्या अभिकारक के मोलों की संख्या से अधिक है तो ∆n धनात्मक होगा तथा ∆H का मान ∆U से अधिक होगा। अतः ∆H = ∆U + ∆nRT
(2) यदि अभिकारक के मोलों की संख्या उत्पाद के मोलों की संख्या से अधिक हो तो ∆n ऋणात्मक होगा तथा ∆H का मान ∆U से कम होगा। ∆H = ∆U – ∆nRT
(3) यदि अभिकारक के मोलों की संख्या उत्पाद के मोलों की संख्या के बराबर हो तो ∆n = 0. इस परिस्थिति में ∆H = ∆U होगा।
![]()
प्रश्न 2.
सिद्ध कीजिए –
qp = ∆Hp .
अथवा, सिद्ध कीजिए कि स्थिर दाब व स्थिर ताप पर अभिक्रिया की ऊष्मा, निकाय के एन्थैल्पी परिवर्तन के बराबर होता है।
उत्तर:
यदि कोई प्रक्रम स्थिर दाब पर हो रहा है तो तंत्र के आयतन में परिवर्तन होता है। यदि तंत्र द्वारा ऊष्मा का अवशोषण हो रहा है जिसके फलस्वरूप आंतरिक ऊर्जा में वृद्धि U1 से U2 हो रही है तथा आयतन में वृद्धि V1 से V2 हो रही है तो ऊष्मागतिकी के प्रथम नियमानुसार,
q = ∆U+ W = ∆U+ P∆V (∴W = P∆V)
या q= [U2 – U1] + P(V2 – V1), [U2 – U1 = ∆U, V2 – V1 =∆V]
या q= [U2 – U1] + [PV2 – PV1]
या q= [U2 + PV2] – [U1 + PV1] ……..(1)
आंतरिक ऊर्जा, दाब तथा आयतन अवस्था परिवर्ती गुण हैं इसलिये इनका योग भी अवस्था परिवर्ती गुण होगा, जिसे एन्थैल्पी कहते हैं तथा H से दर्शाते हैं।
U + PV =H
यदि प्रारंभिक स्थिति में आंतरिक ऊर्जा, आयतन तथा एन्थैल्पी क्रमशः U1V1 तथा H1 हो तो.
U1 + PV1 = H1
इसी प्रकार अंतिम स्थिति में यदि आंतरिक ऊर्जा, आयतन तथा एन्थैल्पी क्रमशः U2, V2तथा H2 हो तो
U2 + PV2 = H2
समीकरण (1) में मान रखने पर,
q= H2 – H1 = ∆Hp.
प्रश्न 3.
हेस का स्थिर ऊष्मा संकलन का नियम समझाइये तथा इसे उदाहरण सहित स्पष्ट कीजिए।
उत्तर:
सन् 1840 में जी. एच. हेस ने इस नियम का प्रतिपादन किया। इसके अनुसार, “किसी भौतिक अथवा रासायनिक परिवर्तन में एन्थैल्पी परिवर्तन हमेशा समान रहता है, चाहे वह परिवर्तन एक पद में हो या कई पदों में। दूसरे शब्दों में, “किसी अभिक्रिया हेतु एन्थैल्पी परिवर्तन हमेशा स्थिर रहता है तथा यह अभिक्रिया के पथ पर निर्भर नहीं करता है।”
सैद्धांतिक स्पष्टीकरण:
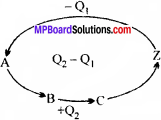
पदार्थ A को उत्पाद x में दो विधियों द्वारा बदला जा सकता है। प्रथम विधि में A को सीधे x में परिवर्तित करने पर मुक्त होने वाली ऊष्मा Q है।
A → x + Q
दूसरी विधि में A को पहले B में, B को C में तथा C को x में बदला जा रहा हो तथा इन पदों में मुक्त होने वाली ऊष्मा क्रमशः q1, q2, q3 हों तो
A → B + q1
B → C + q2
C → x + q3
हेस के नियमानुसार,
Q = q1, q2,q3
उदाहरण:
C को COq2 में निम्नलिखित दो विधियों द्वारा परिवर्तित किया जा सकता हैप्रथम विधि के अनुसार,
C(s) +Q2(g) → CO2(g) ;
∆H = -393.5kJ/mol
द्वितीय विधि द्वारा,
(a) C(s) + \(\frac { 1 }{ 2 }\)O2(g) → CO(g) ; ∆H1 = -110.5 kJ/mol
(b) CO(g) + \(\frac { 1 }{ 2 }\)O2(g) → COCO(g) ; ∆H= -283 kJ/mol
(a) और (b) को जोड़ने पर,
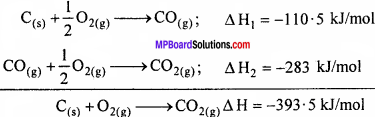
∆H = ∆H1 + ∆H2
![]()
प्रश्न 4.
बम-कैलोरीमीटर द्वारा आन्तरिक ऊर्जा में परिवर्तन AU के निर्धारण की विधि का निम्नलिखित बिन्दुओं के आधार पर वर्णन कीजिए
- उपकरण का नामांकित चित्र
- विधि का वर्णन
- प्रयुक्त सूत्र।
उत्तर:
(1) उपकरण का नामांकित चित्र –
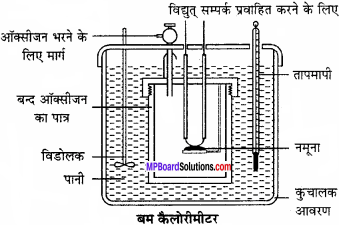
(2) प्रायोगिक निर्धारण:
किसी अभिक्रिया में आन्तरिक ऊर्जा में परिवर्तन का मापन बम कैलोरीमीटर द्वारा करते हैं। यह कठोर स्टील का बना होता है तथा उच्च दाब को सहन कर सकता है। स्टील पात्र के भीतरी सतह में Au या Pt की पालिश रहती है जिससे स्टील का ऑक्सीकरण नहीं हो सकता। स्टील के पात्र में भीतर एक Pt कप में पदार्थ की थोड़ी मात्रा ली जाती है। इस कप में विद्युत् तार लगाये जाते हैं जिससे विद्युत् धारा प्रवाहित करने पर पदार्थ जल जाये।
कप में पदार्थ की अल्प मात्रा लेकर बम कैलोरीमीटर में 20-25 वायुमण्डलीय दाब तक O2 गैस भर लेते हैं तथा बम कैलोरीमीटर को सील कर देते हैं। इसे रुद्धोष्म तंत्र बनाने के लिये ताप रोधित वाटर बाथ में डूबो देते हैं जिसमें भरे हुए जल की मात्रा ज्ञात रहती है। इसमें एक विलोडक तथा एक थर्मामीटर डूबा रहता है। जल का प्रारंभिक ताप नोट कर लेते हैं। विद्युत् स्पार्क उत्पन्न करने से पदार्थ का दहन होता है।
दहन से अत्यन्त ताप द्वारा जलकुण्ड में जल का ताप बढ़ जाता है जिसे नोट कर लिया जाता है। इस तरह ताप में वृद्धि तथा कैलोरीमीटर के जल तुल्यांक के आधार पर अभिक्रिया में उत्पन्न ऊष्मा की गणना कर ली जाती है जो उस अभिक्रिया में आन्तरिक ऊर्जा परिवर्तन ∆U के बराबर होती है।
(3) प्रयुक्त सूत्र:
दहन में उत्पन्न ऊष्मा = कैलोरीमीटर का जल तुल्यांक × ताप में परिवर्तन × जल का विशिष्ट ऊष्माजल तुल्यांक पदार्थ की मात्रा = w gm, पदार्थ का आण्विक द्रव्यमान = m, कैलोरीमीटर का जल तुल्यांक = 2
पदार्थ के दहन से उत्पन्न ऊष्मा = Z×∆t×\(\frac { m }{ w }\)जूल।
प्रश्न 5.
PV कार्य के लिये व्यंजक को व्युत्पन्न कीजिए।
उत्तर:
यदि किसी सिलेण्डर में भारहीन व घर्षणरहित पिस्टन लगा हो जिसके अनुप्रस्थ काट का क्षेत्रफल A है। यदि सिलेण्डर में आदर्श गैस का एक मोल उपस्थित है। गैस का कुल आयतन V तथा दाब P है तथा पिस्टन पर कार्यरत बल F हो तो
![]()
⇒ P = \(\frac { F}{ A }\)
⇒ ∆ × P= F
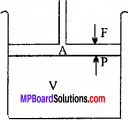
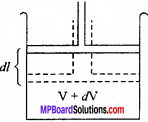
यदि पिस्टन पर कार्यरत बल गैस के दाब की तुलना में कम है तो पिस्टन कुछ L दूरी ऊपर की ओर तय करता है। माना यह विस्थापन वा है। इसके फलस्वरूप आयतन में वृद्धि dl हो रही है तो तंत्र द्वारा किया गया कार्य
कार्य = बल × विस्थापन
W = F × dl
F का मान रखने पर,
w = P × A × dl = Pdv, (A×dl = dV)
यदि आयतन में वृद्धि V2 से V1 हो रही है तो कुल कार्य ज्ञात करने के लिये समाकलन करना पड़ता है अतः
चिह्न का प्रयोग:
यदि तंत्र द्वारा घिराव पर कार्य होता है तो किया गया। कार्य ऋणात्मक होता है क्योंकि कार्य करने में तंत्र की आंतरिक ऊर्जा प्रयुक्त होती है जिसके फलस्वरूप आंतरिक ऊर्जा में कमी आती है। यदि घिराव द्वारा तंत्र पर कार्य किया जाता है तो किया गया कार्य धनात्मक होता है क्योंकि तंत्र की आंतरिक ऊर्जा में वृद्धि होती है।
प्रश्न 6.
मुक्त ऊर्जा किसे कहते हैं ? इसके लिए गणितीय स्वरूप की व्याख्या कीजिए तथा गिब्स-हैल्महोल्ट्ज समीकरण दीजिए।
उत्तर:
मुक्त ऊर्जा (Free Energy):
इसे ‘G’ द्वारा दर्शाया जाता है। यह एक ऐसा उष्मागति की फलन है जिसकी सहायता से किसी तन्त्र के होने या चलने की सम्भावना और उसकी तात्कालिकता (Spontaneity) का आकलन किया जा सकता है। मुक्त ऊर्जा की परिभाषा निम्न प्रकार से दी जा सकती है – किसी तन्त्र से प्राप्त ऊर्जा की वह मात्रा जिसे उपयोगी काम (Useful Work) में लगाया जा सके तन्त्र की मुक्त ऊर्जा कहलाती है। मुक्त ऊर्जा (G) का गणितीय रूप निम्न प्रकार है –
G = H – TH
H = तन्त्र की एन्थैल्पी, S = तन्त्र की एन्ट्रॉपी, T = तापक्रम।
हम जानते हैं कि H = U + PV
G = (U + PV) – TS
तन्त्र के ऊर्जा परिवर्तन (∆G) को निम्नवत दर्शाया जा सकता है –
AG = ∆U+ ∆(PV) – ∆(TS)
यदि प्रक्रम स्थिर दाब और स्थित ताप हो रहा है तो ∆(PV) को P∆V तथा P∆S को T∆S लिखा जायेगा। अतः ∆G = ∆U + P∆V – T∆S
हम जानते हैं कि स्थिर ताप और स्थिर दाब पर,
∆U+ P∆V = ∆H तब ∆G + P∆H = T∆S
गिब्स के समीकरण G = H – TS को स्थिर ताप पर प्रारम्भिक तथा अन्तिम अवस्थाओं के लिए इस प्रकार लिख सकते हैं कि G1 = H1 – TS1 तथा G2 = H2 – TS2
∆G = ∆G1 = ∆G2
अथवा ∆G = (H2 – TS2) – (H1– TS1)
अथवा ∆G = (H2 – H1) – (TS2 – TS1) = ∆H – T∆S
इस समीकरण को गिब्स-हैल्महोल्ट्ज समीकरण कहते हैं।