MP Board Class 11th Chemistry Solutions Chapter 13 हाइड्रोकार्बन
हाइड्रोकार्बन NCERT अभ्यास प्रश्न
प्रश्न 1.
मेथेन के क्लोरीनीकरण के दौरान ऐथेन कैसे बनती है ? आप इसे कैसे समझाएँगे?
उत्तर:
मेथेन का क्लोरीनीकरण मुक्त मूलक क्रियाविधि द्वारा होता है। मेथिल मुक्त मूलक (CH3 ) श्रृंखला समापन पद के दौरान ऐथेन में रूपान्तरित हो जाते हैं।
![]()
प्रश्न 2.
निम्नलिखित यौगिकों के IUPAC नाम लिखिए –
(i) CH3 CH = C(CH3)2
(ii) CH3 = CH – C ≡ C – CH3
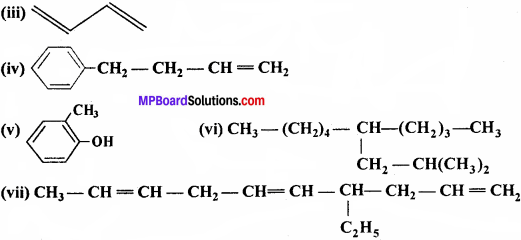
उत्तर:
प्रश्न 3.
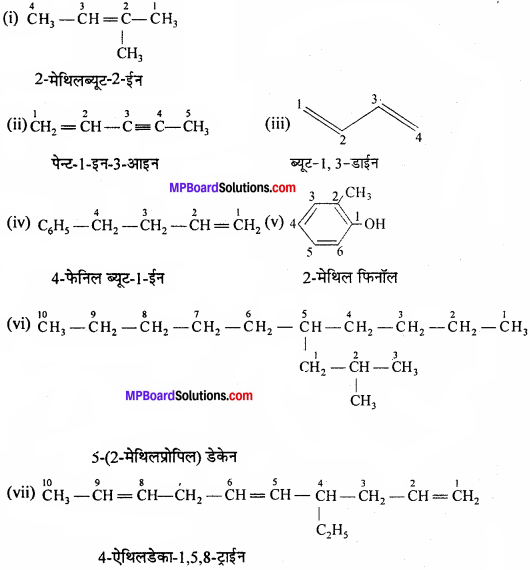
निम्नलिखित यौगिकों, जिनमें द्विआबन्ध तथा त्रिआबन्ध की संख्या दर्शायी गई है, के सभी सम्भावित स्थिति समावयवों के संरचना-सूत्र एवं IUPAC नाम दीजिए –
(a) C4H8 (एक द्विआबन्ध)
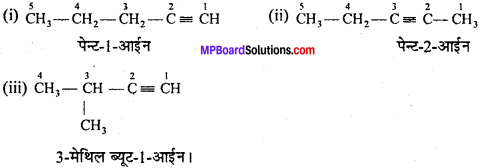
(b) C5H8 (एक त्रिआबन्ध)।
उत्तर:
(a) C4H8 के समावयवी जो द्विआबंध रखते हैं –

(b) C5H8 के समावयवी जो त्रिआबंध रखते हैं –
प्रश्न 4.
निम्नलिखित यौगिकों के ओजोनी-अपघटन के पश्चात् बनने वाले उत्पादों के नाम लिखिए –
(1) पेन्ट-2-ईन
(ii) 3, 4-डाइमेथिलहेप्ट-3-ईन
(iii) 2- एथिलब्यूट-1-ईन
(iv) 1-फेनिलब्यूट-1-ईन।
उत्तर:

प्रश्न 5.
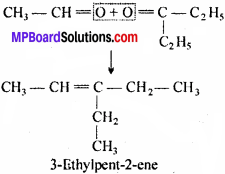
एक ऐल्कीन ‘A’ के ओजोनी अपघटन से पेन्टेन-3-ओन तथा ऐथेनल का मिश्रण प्राप्त होता है। A का IUPAC नाम तथा संरचना दीजिए।
उत्तर:
ओजोनी अपघटन के फलस्वरूप बने उत्पादों की संरचना इस प्रकार लिखते हैं जिससे उनके ऑक्सीजन परमाणु एक दूसरे की ओर इंगित रहे। दोनों ऑक्सीजन परमाणु को निकालने के पश्चात् दोनों सिरों की द्विआबंध से जोड़कर, एल्कीन ‘A’ की संरचना प्राप्त करते है।
प्रश्न 6.
एक ऐल्कीन A में तीन C – C, आठ C – H सिग्मा आबन्ध तथा एक C – C पाई आबन्ध है। A ओजोनी अपघटन से दो अणु ऐल्डिहाइड, जिनका मोलर द्रव्यमान 44 है, देता है। A का आई.यू.मी.ए.सी. नाम लिखिए।
उत्तर:
मोलर द्रव्यमान 44u वाला ऐल्डिहाइड, ऐथेनल (CH3CHO) है। अतः इसके दो अणु की संरचनाओं से –
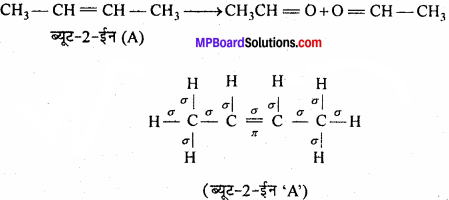
अत: एल्कीन ‘A’ अर्थात् ब्यूट-2-ईन में तीन C-C, आठ C- HO – आबंध तथा एक C – C 2-आबंध उपस्थित है। जो संख्या प्रश्नों में दी गई है।
प्रश्न 7.
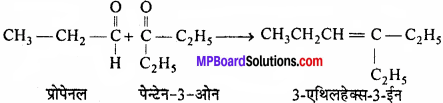
एक एल्कीन, जिसके ओजोनी अपघटन से प्रोपेनल (Propanal) तथा पेन्टेन-3-ओन प्राप्त होते हैं, का संरचनात्मक सूत्र क्या है ?
उत्तर:
प्रोपेनल तथा पेन्टेन-3-ओन में से ऑक्सीजन अलग होकर ये द्वि-बंध द्वारा जुड़ जाते हैं।
प्रश्न 8.
निम्नलिखित हाइड्रोकार्बनों के दहन की रासायनिक अभिक्रिया लिखिए –
(i) ब्यूटेन
(ii) पेन्टीन
(iii) हेक्साइन
(iv) टॉलुईन।
उत्तर:
सभी हाइड्रोकार्बन पूर्ण दहन पर CO2 और H2O देते है।

प्रश्न 9.
हेक्स-2-ईन की समपक्ष (सिस) तथा विपक्ष (ट्रान्स ) संरचनायें बनाइए। इनमें से कौनसे समावयव का क्वथनांक उच्च होता है और क्यों ?
उत्तर:
हेक्स-2-ईन (CH3CH2CH2CH = CHCH3) की समपक्ष तथा विपक्ष समावयव की संरचनाएँ निम्न हैं –
सिस समावयवी में क्वथनांक अपेक्षाकृत उच्च होगा क्योंकि इसके द्विध्रुव-द्विध्रुव अन्योन्य क्रिया का परिणाम, ट्रान्स समावयवी की अपेक्षा अधिक होता है।
प्रश्न 10.
बेंजीन में तीन द्वि-आबन्ध होते हैं, फिर भी यह अत्यधिक स्थायी है, क्यों?
उत्तर:
अनुनाद तथा इलेक्ट्रॉनों के विस्थानीकरण के कारण बेन्जीन अणु अत्यधिक स्थायी होता है।
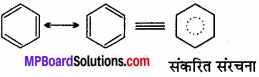
संकरित संरचना संकरित संरचना में बिन्दु वृत्त, बेन्जीन वलय के छ: कार्बन परमाणु पर विस्थानीकृत छ: इलेक्ट्रॉनों को दर्शाता है। अतः विस्थानीकृत छः इलेक्ट्रॉनों की उपस्थिति के कारण बेन्जीन अत्यधिक स्थायी होता है।
प्रश्न 11.
किसी निकाय द्वारा ऐरोमैटिकता प्रदर्शित करने के लिए आवश्यक शर्ते क्या हैं ?
उत्तर:
किसी निकाय का ऐरोमैटिक गुण प्रदर्शित निम्न शर्तों पर निर्भर करता है –
- यौगिक संरचना समतलीय होनी चाहिये।
- यौगिक अनुनादी संरचनायें प्रदर्शित करें।
- यौगिक हकल नियम का पालन करें।
- यौगिक इलेक्ट्रॉन स्नेही अभिक्रियाएँ प्रदर्शित करें
![]()
प्रश्न 12.
इनमें से कौन-से निकाय ऐरोमैटिक नहीं है ? कारण स्पष्ट कीजिए –

उत्तर:
![]()
(a) यह संरचना समतलीय नहीं है क्योंकि इसमें एक C परमाणु sp’ संकरित अवस्था में उपस्थित है।
(b) यह संरचना इलेक्ट्रॉन स्नेही प्रतिस्थापी अभिक्रियाएँ प्रदर्शित नहीं करती।
(ii) ![]()
यह संरचना ऐरोमैटिक गुण प्रदर्शित नहीं करता क्योंकि
(a) इसकी संरचना समतलीय नहीं है (इसमें एक C परमाणु का संकरण अवस्था sp’ है।)
(b) यह हकल नियम का पालन नहीं करता।
(c) यह अनुनादी संरचनायें भी प्रदर्शित नहीं करता।
(d) यह इलेक्ट्रॉन स्नेही प्रतिस्थापी अभिक्रियाएँ नहीं देती।
(ii)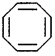
यह संरचना ऐरोमैटिक गुण प्रदर्शित नहीं करता क्योंकि
(a) इसकी संरचना समतलीय नहीं है।
(b) यह संरचना हकल नियम का पालन नहीं करती।।
(c) यह इलेक्ट्रॉन स्नेही प्रतिस्थापी अभिक्रियाएँ प्रदर्शित नहीं करती।
प्रश्न 13.
बेंजीन को निम्नलिखित में कैसे परिवर्तित करेंगे –
- p – नाइट्रोब्रोमोबेंजीन
- m – नाइट्रोक्लोरोबेंजीन
- p – नाइट्रोटॉलुईन
- ऐसीटोफिनोन।
उत्तर:
ये रूपान्तरण इस तथ्य पर आधारित होते हैं कि –
- क्लोरीन की प्रकृति ऑर्थों और पैरा निर्देशी होती है।
- नाइट्रो समूह की प्रकृति मेटा निर्देशी होती है।
1. बेंजीन से p – नाइट्रोनोमोबेंजीन –
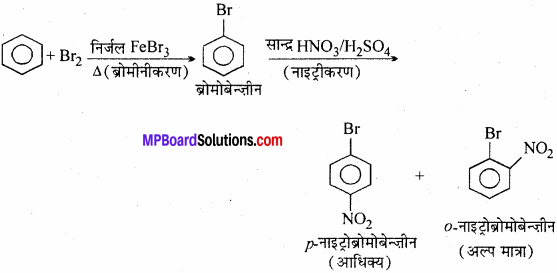
2. बेंजीन से m – क्लोरोनाइट्रोबेंजीन –
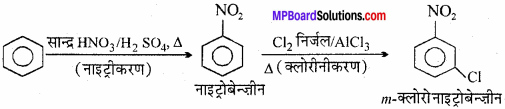
3. बेंजीन से p – नाइट्रोटॉलुईन –
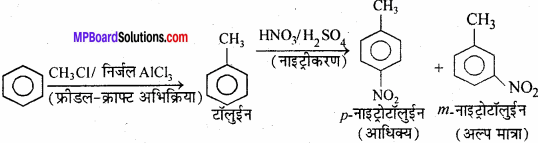
4. बेंजीन से p – एसीटोफिनोन –
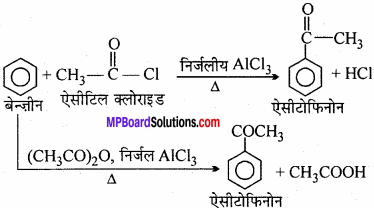
प्रश्न 14.
ऐल्केन H3C – CH2 – C(CH3)2 – CH2– CH(CH3)2 में 1,2° तथा 3° कार्बन परमाणुओं की पहचान कीजिए तथा प्रत्येक कार्बन से आबन्धित कुल हाइड्रोजन परमाणुओं की संख्या भी बताइए।
उत्तर:
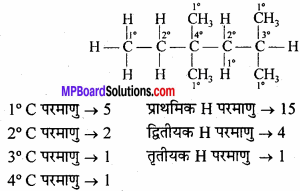
प्रश्न 15.
क्वथनांक पर ऐल्केन की श्रृंखला के शाखन (Branch) का क्या प्रभाव पड़ता है ?
उत्तर:
श्रृंखला में शाखन में वृद्धि के फलस्वरूप पृष्ठ सतह घटता है। अतः एल्केन की श्रृंखला के शाखन में वृद्धि के फलस्वरूप वाण्डर वाल्स आकर्षण बलों में कमी के कारण, क्वथनांक घटता है।
![]()
प्रश्न 16.
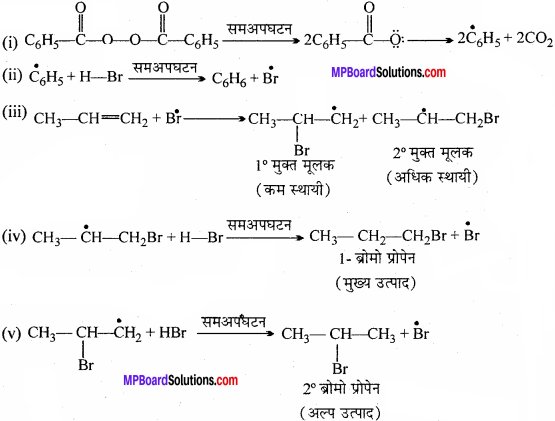
प्रोपीन पर HBr के संकलन से 2-ब्रोमोप्रोपेन बनता है, जबकि बेन्जॉयल परॉक्साइड की उपस्थिति में यह अभिक्रिया 1-ब्रोमोप्रोपेन देती है। क्रियाविधि की सहायता से इसका कारण स्पष्ट कीजिए।
उत्तर:
प्रोपीन (असममित ऐल्कीन) पर HBr योग मार्कोनीकॉफ नियम के अनुसार धनायनिक क्रियाविधि से संपादित होती है। HBr इलेक्ट्रॉन स्नेही, H’ उत्पन्न करता है जो कार्बधनायन से द्विबंध पर आक्रमण करता है।
(i) H – Br → H+ + Br–

इस -2° कार्बधनायन पर Br आयन आक्रमण करके उत्पाद बनाता है।
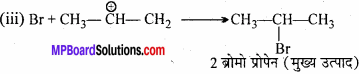
ब्रोमो प्रोपेन (मुख्य उत्पाद) बेन्जॉयल परॉक्साइड की उपस्थिति में प्रोपीन पर HBr का योग मार्कोनीकॉफ नियम के विपरीत होता है। यह मुक्त मूलक की क्रिया से संपादित होता है। इस अभिक्रिया को प्रति मार्कोनीकॉफ योग या परॉक्साइड प्रभाव या खराश प्रभाव कहते हैं। यह केवल HBr के साथ होता है, HCl तथा HI के साथ नहीं। क्रियाविधि निम्न हैं –
प्रश्न 17.
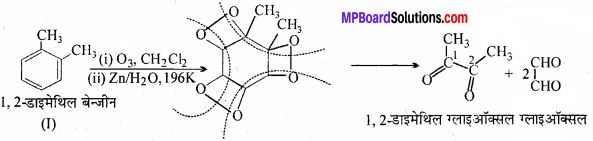
1, 2-डाइमेथिलबेंजीन (o – जाइलीन) के ओजोनी अपघटन के फलस्वरूप निर्मित उत्पादों को लिखिए। यह परिणाम बेंजीन की केकुले संरचना की पुष्टि किस प्रकार करता है ?
उत्तर:
इसी प्रकार,
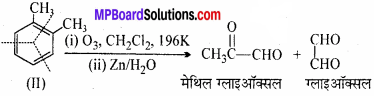
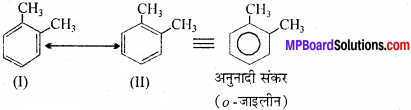
ये तीनों उत्पाद दोनों कैकुले संरचनाओं में से किसी एक द्वारा ही नहीं प्राप्त किए जा सकते है। इससे प्रदर्शित होता है कि o-जाइलीन, वास्तव में दो कैकुले संरचनाओं ग्लाइऑक्सल (I तथा II) का अनुनादी रूप है।
प्रश्न 18.
बेंजीन, n – हेक्सेन तथा एथाइन को घटते हुए अम्लीय व्यवहार के क्रम में व्यवस्थित कीजिए और इस व्यवहार का कारण बताइए।
उत्तर:
अम्लीय सामर्थ्य का घटता हुआ क्रम है –

अम्लीय अभिलक्षण S-अभिलक्षण की प्रतिशतता से सम्बन्धित होता है। 5-अभिलक्षण जितना अधिक होता है, कार्बन परमाणु की वैद्युत ऋणात्मकता उतनी ही अधिक होती है तथा उसका अम्लीय अभिलक्षण भी उतना ही अधिक होगा।
प्रश्न 19.
बेंजीन इलेक्ट्रॉनस्नेही प्रतिस्थापन अभिक्रियाएँ सरलतापूर्वक क्यों प्रदर्शित करती है, जबकि उसमें नाभिकस्नेही प्रतिस्थापन कठिन होता है ?
उत्तर:
बेंजीन में द्विआबन्धों को प्रदर्शित करने वाले तीन T – इलेक्ट्रॉनों युग्मों के कारण इलेक्ट्रॉन घनत्व उच्च होता है। यद्यपि इलेक्ट्रॉन आवेश अनुनाद के कारण बहुत अधिक विस्थानीकृत हो जाता है, तथापि इसमें इलेक्ट्रॉनस्नेही प्रतिस्थापन कराने वाला इलेक्ट्रॉन-स्नेही आक्रमण सम्भव होता है। किन्तु, बेंजीन नाभिकस्नेही प्रतिस्थापन के प्रति अनुक्रियाशील नहीं होता है क्योंकि नाभिकस्नेही प्राथमिकता के तौर पर कम इलेक्ट्रॉन घनत्व के केन्द्र पर आक्रमण करता है।
![]()
प्रश्न 20.
आप निम्नलिखित यौगिकों को बेंजीन में कैसे परिवर्तित करेंगे –
- एथाइन
- एथीन
- हेक्सेन।
उत्तर:
1. एथाइन से बेंजीन –

2. एथीन से बेंजीन –
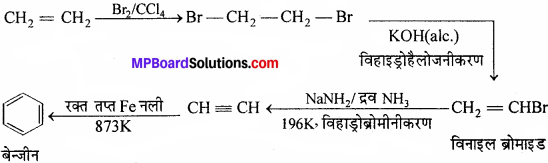
3. हेक्सेन से बेंजीन –
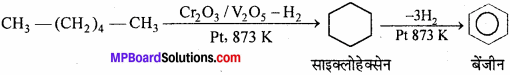
प्रश्न 21.
उन सभी एल्कीनों की संरचनाएँ लिखिए, जो हाइड्रोजनीकरण करने पर 2-मेथिलब्यूटेन देती हैं।
उत्तर:
उपर्युक्त प्रश्न को हम निम्न प्रकार से मालूम करेंगे –
2-मेथिलब्यूटेन प्राप्त करने के लिये कौन-सी एल्कीन लेनी होगी –
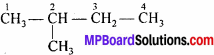
उपर्युक्त संरचना को हमें एल्कीन से प्राप्त करनी है। उपर्युक्त संरचना में पास-पास वाले C परमाणुओं से H परमाणु हटा कर द्विबन्ध जोड़ दें।

प्रश्न 22.
निम्नलिखित यौगिकों को उनकी इलेक्ट्रॉनस्नेही (E’) के प्रति घटती सापेक्षिक अभिक्रियाशीलता के क्रम में व्यवस्थित कीजिए –
1. क्लोरोबेंजीन, 2-4-डाइनाइट्रोक्लोरोबेंजीन, p-नाइट्रो-क्लोरोबेंजीन
2. टॉलुईन, P – H3C – C6H4 – NO2, P – O2N – C6H4 – NO2
उत्तर:
1. इलेक्ट्रॉनस्नेही प्रतिस्थापन के प्रति अभिक्रियाशीलता का घटता हुआ सही क्रम है –
क्लोरोबेंजीन >p-नाइट्रोक्लोरोबेंजीन >2,4-डाईनाइट्रोक्लोरोबेंजीन
नाइट्रो समूह (NO2) एक विसक्रियकारी समूह है। बेंजीन वलय पर इसकी उपस्थिति इसे इलेक्ट्रॉनस्नेही आक्रमण के प्रति विसक्रियित करेगी, क्योंकि इलेक्ट्रॉनस्नेही उच्च इलेक्ट्रॉन घनत्व के केन्द्र की खोज करता है। अतः नाइट्रो समूहों की संख्या जितनी ही अधिक होगी, इलेक्ट्रॉनस्नेही प्रतिस्थापन के प्रति यौगिकों की अभिक्रियाशीलता उतनी ही कम होगी।
2. घटती हुई अभिक्रियाशीलता का सही क्रम है – .
टॉलुईन > p – नाइट्रोटॉलुईन > p – डाईनाइट्रोबेंजीन
मेथिल समूह एक सक्रियकारी समूह है, जबकि नाइट्रो समूह की प्रकृति विसक्रियकारी होती है। इस तथ्य के प्रकाश में इलेक्ट्रॉनस्नेही आक्रमण के प्रति अभिक्रियाशीलता का घटता हुआ यह क्रम तर्कसंगत सिद्ध होता है –
टॉलुईन > बेंजीन > m-डाईनाइट्रोबेंजीन
प्रश्न 23.
बेंजीन, m – डाइनाइट्रोबेंजीन और टॉलुईन में से किसका नाइट्रीकरण आसानी से होता है। और क्यों ?
उत्तर:
बेंजीन के नाइट्रीकरण में वलय पर \(\mathrm{NO}_{2}^{\ominus}\) (नाइट्रोनियम आयन) का इलेक्ट्रॉनस्नेही आक्रमण होता है। चूंकि CH3 समूह में +I प्रभाव होता है, इसलिए यह वलय को सक्रिय कर देता है और इसका इलेक्ट्रॉनस्नेही प्रतिस्थापन आसानी से होता है। दूसरी ओर, नाइट्रो समूह की विसक्रियकारी प्रकृति के कारण यह m-डाइनाइट्रोबेंजीन में सबसे कठिनाई से होता है। इस प्रकार टॉलुईन का नाइट्रीकरण सबसे आसानी से होगा। टॉलुईन > बेंजीन > m – डाईनाइट्रोबेंजीन
प्रश्न 24.
बेंजीन के एथिलीकरण में निर्जल ऐल्युमिनियम क्लोराइड के स्थान पर कोई दूसरा लुईस अम्ल सुझाइए।
उत्तर;
निर्जल फेरिक क्लोराइड (FeCl5) वह अन्य लुईस अम्ल है जिसे प्रयुक्त कर सकते हैं। यह इलेक्ट्रॉनस्नेही (C2H5ई) पैदा करने में सहायक होता है। स्टेनिक क्लोराइड (SnCl4) एवं बोरॉन ट्राइफ्लुओराइड (BF3) . का भी प्रयोग किया जा सकता है।
प्रश्न 25.
क्या कारण है कि वुर्ट्ज अभिक्रिया से विषम संख्या कार्बन परमाणु वाले विशुद्ध ऐल्केन बनाने के लिए प्रयुक्त नहीं की जाती? एक उदाहरण देकर स्पष्ट कीजिए।
उत्तर:
कार्बन परमाणुओं की विषम संख्या वाले ऐल्केन के निर्माण में दो भिन्न-भिन्न हैलोऐल्केन आवश्यक होते हैं, जिनमें से एक में कार्बन परमाणुओं की विषम संख्या हो और दूसरे में सम संख्या हो। उदाहरण के लिए ब्रोमोएथेन और 1-ब्रोमोप्रोपेन इस अभिक्रिया के फलस्वरूप पेन्टेन देंगे।
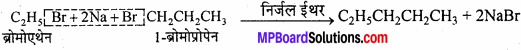
परन्तु जब इस अभिक्रिया में भाग लेने वाले सदस्य अलग-अलग अभिक्रिया करेंगे तो पार्श्व उत्पाद भी बनेंगे। उदाहरण के लिए, ब्रोमोएथेन, ब्यूटेन देता है और 1- ब्रोमोप्रोपेन, हेक्सेन देता हैं।
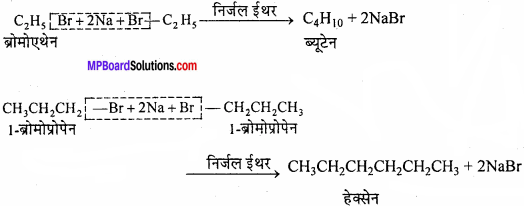
इस प्रकार ब्यूटेन, पेन्टेन और हेक्सेन का मिश्रण बनेगा। इस मिश्रण से इनके घटकों को पृथक् करना काफी कठिन होगा।
हाइड्रोकार्बन अन्य महत्वपूर्ण प्रश्न
हाइड्रोकार्बन वस्तुनिष्ठ प्रश्न
प्रश्न 1.
सही विकल्प चुनकर लिखिए –
प्रश्न 1.
मेथेन में H – C – H बन्ध कोण है –
(a) 100°5′
(b) 109°
(c) 109°28′
(d) 180°
उत्तर:
(c) 109°28′
प्रश्न 2.
C = C में है –
(a) 30 बन्ध
(b) एक सिग्मा और तीन पाई बन्ध
(c) 37 बन्ध
(d) एक सिग्मा और दो पाई बन्ध
उत्तर:
(d) एक सिग्मा और दो पाई बन्ध
प्रश्न 3.
एथीन में है –
(a) पाँच सिग्मा और एक पाई बन्ध
(b) छ: सिग्मा बन्ध
(c) चार सिग्मा और दो पाई बन्ध
(d) पाँच सिग्मा बन्ध।
उत्तर:
(a) पाँच सिग्मा और एक पाई बन्ध
![]()
प्रश्न 4.
किसकी क्रियाशीलता सर्वाधिक है –
(a) C2H2
(b) CH4
(c) C2H4
(d) C2H6.
उत्तर:
(a) C2H2
प्रश्न 5.
ज्यामितीय समावयवता प्रदर्शित करता है –
(a) ब्यूट-2-ईन
(b) ब्यूट-2-आइन
(c) ब्यूटेन-2-ऑल
(d) ब्यूटेनल।
उत्तर:
(a) ब्यूट-2-ईन
प्रश्न 6.
बेंजीन में कार्बन द्वारा उपयोग में लाई गई प्रसंकरित ऑर्बिटल (कक्षक) होती है –
(a) sp3
(b) sp2
(c) sp
(d) dsp3
उत्तर:
(b) sp2
प्रश्न 7.
HC ≡ C – CH = CH, के C – C एक आबन्ध के कार्बन परमाणुओं का संकरण है –
(a) sp3 – sp3
(b) sp2 – sp3
(c) sp3 – sp
(d) sp – sp2
उत्तर:
(d) sp – sp2
प्रश्न 8.
ब्यूट-1-इन में सिग्मा बन्धों की संख्या है –
(a) 8
(b) 10
(c) 11
(d) 12.
उत्तर:
(c) 11
प्रश्न 9.
एथिलीन में उपस्थित दो परमाणुओं के मध्य विद्यमान द्विबन्ध होता है –
(a) लम्बवत् दो सिग्मा-बन्ध
(b) एक सिग्मा (σ) तथा एक पाई (π) बन्ध
(c) लम्बवत् दो पाई-बन्ध
(d) 60 अंश का कोण बनाते हुए दो पाई-बन्ध।
उत्तर:
(b) एक सिग्मा (σ) तथा एक पाई (π) बन्ध
प्रश्न 10.
निम्न में से कौन-सा अभिकर्मक एथिलीन और ऐसीटिलीन में विभेद करता है –
(a) जलीय क्षारीय KMnO4
(b) CCl4 में Cl2 विलेय
(c) अमोनियामय Cu2 Cl2
(d) सान्द्र H2SO4
उत्तर:
(c) अमोनियामय Cu2Cl2
प्रश्न 11.
इंजन में अपस्फोटी ध्वनि उत्पन्न होती है, जब ईंधन –
(a) धीरे जलता है
(b) तेजी से जलता है
(c) पानी होता है
(d) मशीन तेल मिश्रित होता है।
उत्तर:
(b) तेजी से जलता है
![]()
प्रश्न 12.
ईंधन का अपस्फोटक गुण बढ़ाने के लिये मिलाया जाता है –
(a) PbBr2
(b) ZnBr2
(c) Pbo
(d) TEL (Tetraethyl lead).
उत्तर:
(d) TEL (Tetraethyl lead).
प्रश्न 13.
मेथेन बनाने के लिए निम्न में से किस विधि का उपयोग किया जा सकता है –
(a) वु अभिक्रिया
(b) कोल्बे अभिक्रिया
(c) ऐल्किल हैलाइड का अपचयन
(d) ऐल्कीन का हाइड्रोजनीकरण।
उत्तर:
(c) ऐल्किल हैलाइड का अपचयन
प्रश्न 14.
जब ऐसीटिलीन HCl की उपस्थिति में HgCl2 से अभिक्रिया करती है, तो बनता है
(a) मेथिल क्लोराइड
(b) ऐसीटैल्डिहाइड
(c) वाइनिल क्लोराइड
(d) फॉर्मेल्डिहाइड।
उत्तर:
(b) ऐसीटैल्डिहाइड
प्रश्न 15.
जब प्रोपाइन को HgSO4 की उपस्थिति में जलीय H2 SO4 से प्रतिकृत किया जाता है, तो मुख्य उत्पाद बनता है –
(a) प्रोपेनल
(b) प्रोपिल हाइड्रोजन सल्फेट
(c) ऐसीटोन
(d) प्रोपेनॉल।
उत्तर:
(c) ऐसीटोन
प्रश्न 16.
प्रोपीन तथा प्रोपाइन में विभेद करने के लिए प्रयुक्त अभिकर्मक है –
(a) ब्रोमीन
(b) क्षारीय KMnO4
(c) अमोनियामय AgNO3
(d) ओजोन।
उत्तर:
(b) क्षारीय KMnO4
![]()
प्रश्न 17.
![]()
(a) वुज अभिक्रिया
(b) कोल्बे अभिक्रिया
(c) साबात्ये सेण्डेरेन्स अभिक्रिया
(d) कार्बिल-ऐमीन अभिक्रिया
उत्तर:
(c) साबात्ये सेण्डेरेन्स अभिक्रिया
प्रश्न 18.
अमोनियाकृत सिल्वर नाइट्रेट विलयन से अभिक्रिया करके C2 H2 बनाता है –
(a) सिल्वर दर्पण
(b) सिल्वर ऑक्साइड
(c) सिल्वर फॉर्मेट
(d) सिल्वर ऐसीटिलाइड।
उत्तर:
(d) सिल्वर ऐसीटिलाइड।
प्रश्न 19.
एक अज्ञात यौगिक A का अणु सूत्र C4 H6 है । जब Aकी ब्रोमीन की अधिक मात्रा से अभि क्रिया करायी जाती है, एक नया पदार्थ B बनता है जिसका अणुसूत्र C4 H6 Br4 है। A अमोनिया युक्त AgNO3 के साथ सफेद अवक्षेप देता है। A हो सकता है –
(a) ब्यूट-1-आइन
(b) ब्यूट-2-आइन
(c) ब्यूट-1-ईन
(d) ब्यूट-2-ईन।
उत्तर:
(b) ब्यूट-2-आइन
प्रश्न 20.
क्रियाशीलता बढ़ाने वाले समूह होते हैं –
(a) o-,p-निर्देशकारी समूह
(b) m-निर्देशकारी समूह
(0) NO2
(d) इनमें से कोई नहीं।
उत्तर:
(a) o-,p-निर्देशकारी समूह
प्रश्न 21.
निम्नलिखित में से कौन-सा एल्केन, वु अभिक्रिया द्वारा प्राप्त नहीं होता है –
(a) CH4
(b) C2H6
(c) C3H8
(d) C4H10
उत्तर:
(a) CH4
प्रश्न 22.
निम्न में प्रति ऐरोमैटिक है –
(a) बेंजीन
(b) साइक्लोऑक्टाडाईन
(c) ट्रोपोलियम धनायन
(d) साइक्लोपेन्टाडाइनील धनायन।
उत्तर:
(d) साइक्लोपेन्टाडाइनील धनायन।
![]()
प्रश्न 2.
रिक्त स्थानों की पूर्ति कीजिये –
- कैरोसीन तेल …………. का मिश्रण है।
- ………… में कार्बन-कार्बन बन्ध लम्बाई न्यूनतम होती है।
- प्रोपीन तथा प्रोपाइन में विभेद करने के लिए ………… अभिकर्मक प्रयुक्त किया जाता है।
- टेफ्लॉन …………. का बहुलक है।
- एथेनॉल के निर्जलीकरण से ………… बनता है।
- बेंजीन H2 से योग करके …………. बनाता है।
- ज्यामितीय समावयवता ……………… में पायी जाती है।
- सर्वाधिक स्थायी संरूपी …………… रूप होता है।
- विपक्ष समावयवी, समरूप समावयवी से …………. स्थायी होता है।
- ऐल्युमीनियम कार्बाइड की जल से अभिक्रिया कराने पर …………. प्राप्त होता है।
उत्तर:
- एल्केन
- एथाइन
- बेयर अभिकर्मक (क्षारीय KMnO4)
- टेट्रा फ्लोरो एथिलीन
- एथीन
- साइक्लोहेक्सेन
- ऐल्कीन
- सांतरित
- अधिक
- CH4
![]()
प्रश्न 3.
उचित संबंध जोडिए –

उत्तर:
- (b) कोल्बे अभिक्रिया
- (d) वु अभिक्रिया से
- (e) मेथेन।
- (a) इलेक्ट्रॉन स्नेही प्रतिस्थापन अभिक्रिया
- (c) sp – संकरण

उत्तर:
- (e) पार्श्व अतिव्यापन
- (a) इलेक्ट्रॉन स्नेही प्रतिस्थापन
- (1) 0, p समूह
- (b) असंतृप्त हाइड्रोकार्बन
- (c) द्रवीभूत पेट्रोलियम गैस
- (g) कम्प्रेस्ड नेचुरल गैस
- (d) समपक्ष-विपक्ष समावयवी
![]()
प्रश्न 4.
एक शब्द / वाक्य में उत्तर दीजिए –
1. T.E.L. का पूरा नाम है।
2. एथिलीन डाइ ब्रोमाइड को Zn चूर्ण के साथ गर्म करने पर क्या बनता है?
3. L.P.G. में दुर्गन्ध पैदा करने वाले पदार्थ का नाम बताइये।
4. पोटैशियम एसीटेट के जलीय विलयन के विद्युत् अपघटन से एथेन बनता है, इस विधि का नाम बताइए।
5. ![]()
6. 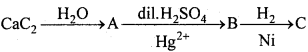
प्रश्न 7.
एल्किल हैलाइड व सोडियम से ऐल्केन बनाने के लिए प्रयुक्त अभिक्रिया का नाम लिखिए।
उत्तर:
1. टेट्रा एथिल लेड
2. एथिलीन
3. एथिल मर्केप्टेन
4. कोल्बे अभिक्रिया
5. साबात्ये सेण्डरेन्स अपचयन अभिक्रिया
6. (A) CH = CH, (B) CH3 – CHO, (C) CH3– CH2– OH
7. वु फिटिग अभिक्रिया।
हाइड्रोकार्बन अति लघु उत्तरीय प्रश्न
प्रश्न 1.
ऐल्काइन के द्रव अमोनिया में सोडियम द्वारा अपचयन के फलस्वरूप विपक्ष ऐल्कीन बनती है। क्या 2-ब्यूटाइन के इस प्रकार हुए अपचयन के फलस्वरूप ब्यूटीन ज्यामितीय समावयवता प्रदर्शित करेगी?
उत्तर:
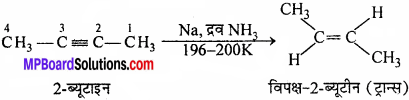
2-ब्यूटाइन के अपचयन से प्राप्त विपक्ष-2-ब्यूटीन ज्यामितीय समावयवता प्रदर्शित करती है।
प्रश्न 2.
-1 प्रभाव के बावजूद, हैलोजन, हैलोएरीन यौगिकों में 0 – (ऑर्थो) तथा p – (पैरा) निर्देशी होती है। कारण स्पष्ट कीजिए।
उत्तर:
हैलोजन अत्यधिक निष्क्रिय समूह है। इनके प्रबल – I प्रभाव के कारण बेन्जीन वलय पर इलेक्ट्रॉन घनत्व घटता है। परन्तु अनुनाद के कारण o – तथा p – स्थानों पर इलेक्ट्रॉन घनत्व m – स्थान की अपेक्षा अधिक होता है। जिसके कारण ये o – तथा p – निर्देशी समूह होते हैं।
प्रश्न 3.
एल्केनों से एल्कीन की अधिक क्रियाशीलता का क्या कारण है ?
उत्तर:
एल्केनों में C – C के मध्य केवल आबन्ध होता है। जबकि एल्कीन में C = C के मध्य एक – आबन्ध और एक आबंध होता है। पार्वीय अतिव्यापन के कारण π बंध, σ बंध से दुर्बल होता है। इस कारण ऐल्कीन, ऐल्केनों से अधिक क्रियाशील है। 1 आबंध की आबन्ध ऊर्जा (251 kJ/mol) σ आबंध की आबंध ऊर्जा (347kJ/mol) से कम होने के कारण भी इनकी क्रियाशीलता ऐल्केन से अधिक होती है।
प्रश्न 4.
असममित कार्बन किसे कहते हैं ?
उत्तर:
वह कार्बन परमाणु जिससे चार भिन्न समूह या परमाणु जुड़े रहते हैं। असममित कार्बन परमाणु कहलाता है। इस असममित कार्बन की उपस्थिति के कारण यौगिक असममिति दर्शाता है तथा प्रकाश घूर्णकता का गुण दर्शाता है।
प्रश्न 5.
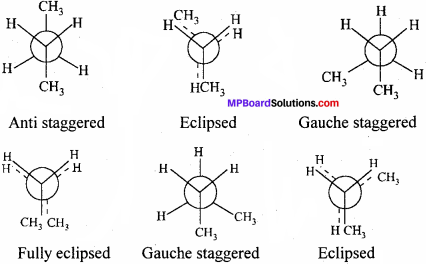
ब्यूटेन के ग्रसित तथा सांतरित संरूपों का न्यूमैन प्रक्षेप आरेख दीजिए।
उत्तर:
ब्यूटेन का संरचना सूत्र –
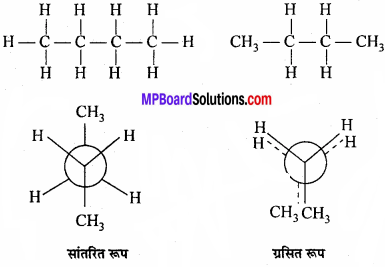
प्रश्न 6.
किरेलता से क्या समझते हो?
उत्तर:
वे अणु जो अपने दर्पण प्रतिबिम्ब पर अध्यारोपित नहीं होते हैं किरेल अणु कहलाते हैं तथा इस गुण को किरेलता कहते हैं। किरेल अणु ध्रुवण घूर्णक होते हैं। अणु में उपस्थित किरेलता असममित कार्बन परमाणु की उपस्थिति के कारण होती है। जिन अणुओं में किरेलता होती है वे ध्रुवण घूर्णक होते हैं लेकिन असममित कार्बन परमाणु युक्त अणु में ध्रुवण घूर्णकता हो यह जरूरी नहीं है। वे ध्रुवण घूर्णक हो भी सकते हैं और नहीं भी।
![]()
प्रश्न 7.
ऐल्केन किसे कहते हैं ? तथा इनमें किस प्रकार के बंध होते हैं ?
उत्तर:
ऐल्केन संतृप्त हाइड्रोकार्बन हैं। इन्हें पैराफिन भी कहते हैं। ये अत्यन्त कम क्रियाशील होते हैं तथा अधिक स्थायी होते हैं। इनका सामान्य सूत्र – CnH2n+2होता है। ऐल्केन में कार्बन – कार्बन के मध्य एकल बंध व 6 बंध होता है तथा कार्बन-हाइड्रोजन बंध भी बंध होता है। ऐल्केन में प्रत्येक कार्बन sp3 संकरित अवस्था में होता है।
उदाहरण – मेथेन CH4एथेन C2H6
प्रश्न 8.
ऐल्कीन किसे कहते हैं ? इनमें कार्बन किस संकरित अवस्था में होता है ?
उत्तर:
ऐल्कीन असंतृप्त हाइड्रोकार्बन होते हैं। इन्हें ओलीफिन भी कहते हैं। ये ऐल्केन की तुलना में अधिक क्रियाशील होते हैं तथा इनका स्थायित्व ऐल्केन की तुलना में कम होता है। ये सरलता से योगात्मक अभिक्रिया देते हैं। इनका सामान्य सूत्र CnH2n – 2 होता है। ऐल्कीन में कार्बन-कार्बन के बीच द्विबंध होता है तथा कार्बन sp संकरित अवस्था में होता है। उदाहरण – एथिलीन CH2 = CH2 प्रोपीलीन CH3 – CH = CH2
प्रश्न 9.
ऐल्काइन किसे कहते हैं ? तथा इनमें किस प्रकार के बंध होते हैं
उत्तर:
ऐल्काइन असंतृप्त हाइड्रोकार्बन होते हैं। ये अत्यधिक क्रियाशील होते हैं तथा अत्यधिक अस्थायी होते हैं। इनका सामान्य सूत्र CnH2n+1 होता है।
कार्बन – कार्बन के मध्य त्रिबंध होता है। जिसमें एक बंध व दो 7 बंध होते हैं तथा दोनों कार्बन sp संकरित अवस्था में होते हैं।
उदाहरण – एसीटिलीन CH = CH, प्रोपाईन CH3 – C ≡ CH2
प्रश्न 10.
समपक्ष-विपक्ष समावयवता क्या होती है ? उदाहरण सहित समझाइये।
उत्तर:
समपक्ष-विपक्ष समावयवता को ज्यामितीय समावयवता भी कहते हैं, जो युग्म बंध युक्त ऐसे यौगिकों के द्वारा दर्शायी जाती है, जिनमें युग्म बन्धित कार्बन परमाणु दो भिन्न परमाणुओं या समूहों द्वारा जुड़े रहते हैं। जब समान समूह या हाइड्रोजन परमाणु द्विबंध के एक ही ओर स्थित होते हैं तो प्राप्त यौगिक समपक्ष समावयवयी तथा जब विपरीत ओर स्थित होते हैं, तो प्राप्त यौगिक विपक्ष समावयवयी कहलाता है।
उदाहरण – CH3 CH = CH – CH3
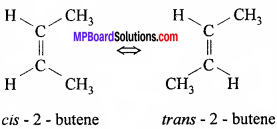
प्रश्न 11.
ऐसीटिलीन से नाइट्रोबेन्जीन आप किस प्रकार प्राप्त करोगे?
उत्तर:
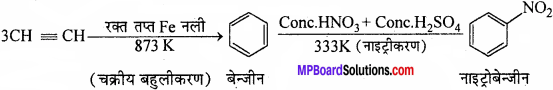
प्रश्न 12.
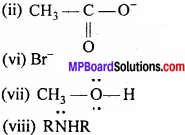
इलेक्ट्रॉन स्नेही तथा नाभिक स्नेही क्रमशः इलेक्ट्रॉन न्यून तथा इलेक्ट्रॉन समृद्ध अभिक्रिया मध्यवर्ती है। अतः इनकी प्रवृत्ति क्रमशः इलेक्ट्रॉन समृद्ध तथा इलेक्ट्रॉन न्यून नाभिकों पर आक्रमण करने की होती है। निम्नलिखित स्पीशीज को इलेक्ट्रॉन स्नेही तथा नाभिक स्नेही के रूप में वर्गीकृत कीजिए –
(i) H3CO–
(iii) Cl
(iv) Cl2C:
(v) (CH3)3C+
(vi) Br–
(vii) CH3OH,
(viii) R – NH – R
उत्तर:
इलेक्ट्रॉन स्नेही, इलेक्ट्रॉन न्यून स्पीशीज होते हैं। ये उदासीन या धनावेशित हो सकते हैं।
(iii) Cl,
(iv) Cl2C:
(v) (CH3)3C
नाभिक स्नेही, इलेक्ट्रॉन समृद्ध स्पीशीज होते है। ये उदासीन या ऋणावेशित हो सकते हैं।
(i) CH3O
प्रश्न 13.
साइक्लोहेक्सेन की तुलना में साइक्लोप्रोपेन अधिक क्रियाशील होता है, क्यों ?
उत्तर:
साइक्लोप्रोपेन में C – C – C बंध कोण 60° का होता है, जिसके कारण वलय तनाव में होता है इसलिये इसका स्थायित्व कम तथा क्रियाशीलता अधिक होती है। जबकि साइक्लोहेक्सेन में C – C – C बंध कोण 109°28 के पास होता है, जिसके कारण वलय का तनाव कम होता है, जिसके कारण इसका स्थायित्व अधिक और क्रियाशीलता कम होती है।
![]()
प्रश्न 14.
क्रियात्मक समावयवता को उदाहरण सहित समझाइये।
उत्तर:
जब दो या दो से अधिक यौगिकों में अलग-अलग क्रियात्मक समूह उपस्थित हों पर उनका अणुसूत्र एक ही हो तो इस प्रकार उत्पन्न समावयवता को क्रियात्मक समावयवता कहते हैं।
उदाहरण – C2H6O
CH3 – O – CH2 ⇔ C2H5 – OH.
प्रश्न 15.
वियोजन क्या है ?
उत्तर:
उपयुक्त विधियों द्वारा रेसेमिक मिश्रण को d या ! प्रतिबिम्ब समावयवयी में पृथक् करने की विधि को वियोजन कहते हैं। इसके लिये यौगिक, जीव रासायनिक एवं रासायनिक विधियों द्वारा वियोजन किया जा सकता है।
प्रश्न 16.
एरीन में कौन-सी समावयवता पायी जाती है ? उदाहरण सहित स्पष्ट कीजिए।
उत्तर:
एरीन में स्थिति समावयवता पायी जाती है। टॉलुईन के अतिरिक्त सभी बेंजीन के यौगिकों में स्थिति समावयवता होती है।
उदाहरण – C8H10 चार समावयवयी रूपों में मिलता है
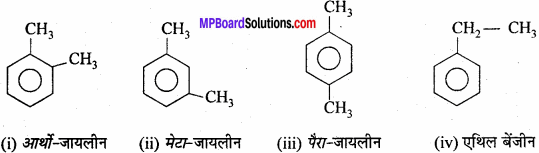
प्रश्न 17.
ऐल्काइन की अम्लीय प्रकृति को दर्शाने के लिये एक अभिक्रिया लिखिए।
उत्तर:
वे ऐल्काइन जिनके अणु के अंतिम छोर में त्रिबंध होता है, वे दुर्बल अम्ल की तरह कार्य करते हैं । ऐसे ऐल्काइन की अभिक्रिया Na, Ca जैसी क्रियाशील धातुओं से कराने पर ये हाइड्रोजन मुक्त करते हैं तथा इनके व्युत्पन्न प्राप्त होते हैं, जिन्हें एसीटिलाइड कहते हैं।
प्रश्न 18.
बेयर अभिकर्मक क्या है, तथा इससे असंतृप्तता का परीक्षण कैसे करते हैं ?
उत्तर:
क्षारीय KMnO4 को बेयर अभिकर्मक कहते हैं। असंतृप्त हाइड्रोकार्बन की अभिक्रिया बेयर अभिकर्मक से कराने पर क्षारीय KMnO4 का रंग उड़ जाता है। इसलिये इसका उपयोग यौगिक की असंतृप्तता के परीक्षण के लिये करते हैं।
प्रश्न 19.
ऐल्कीन पर बेयर अभिकर्मक की अभिक्रिया को समीकरण सहित स्पष्ट कीजिए।
उत्तर:
एथिलीन कमरे के ताप पर 1% क्षारीय KMnO4 अर्थात् बेयर अभिकर्मक के साथ अभिक्रिया कराने पर एथिलीन ग्लाइकॉल बनाता है तथा इस योगात्मक अभिक्रिया के कारण KMnO4 का गुलाबी रंग उड़ जाता है।

प्रश्न 20.
परॉक्साइड प्रभाव क्या है ? एक उदाहरण दीजिए।
उत्तर:
यदि कार्बनिक परॉक्साइड जैसे बेंजॉयल परॉक्साइड की उपस्थिति में असममित एल्कीन या एल्काइन पर असममित अभिकर्मक का योग कराया जाता है तो अभिक्रिया मार्कोनीकॉफ नियम के विपरीत होती है। इस अभिक्रिया को प्रति मार्कोनीकॉफ नियम या परॉक्साइड प्रभाव या खराश प्रभाव कहते हैं।
![]()
प्रश्न 21.
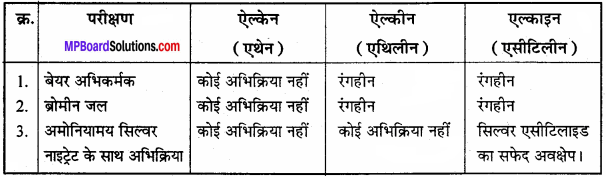
एथेन, एथिलीन तथा एसीटिलीन में विभेद कैसे करते हैं ? परीक्षण सहित समझाइए।
उत्तर:
एथेन, एथिलीन तथा एसीटिलीन में विभेद –
प्रश्न 22.
बर्थलोट संश्लेषण क्या है ?
उत्तर:
दो कार्बन इलेक्ट्रोड के बीच विद्युत् आर्क में से हाइड्रोजन गैस की धारा प्रवाहित करने पर एसीटिलीन प्राप्त होता है। इसे बर्थलोट संश्लेषण कहते हैं।
![]()
प्रश्न 23.
वेस्ट्रॉन तथा वेस्ट्रॉसोल क्या है ?
उत्तर:
(1) ऐसीटिलीन पर CCl4, विलायक की उपस्थिति में हैलोजन की योगात्मक अभिक्रिया से बना .. यौगिक वेस्ट्रॉन कहलाता है।

(2) वेस्ट्रॉन को ऐल्कोहॉलिक KOH के साथ गर्म किया जाता है तो विहाइड्रो – हैलोजनीकरण के कारण वेस्ट्रॉसोल प्राप्त होता है।

प्रश्न 24.
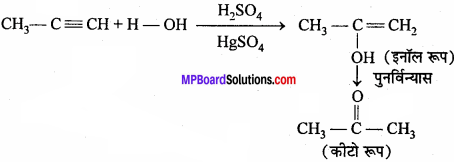
प्रोटोट्रॉफी किसे कहते हैं ?
उत्तर:
प्रोपाइन पर जलयोजन होने पर इनॉल व कीटो रूप प्राप्त होते हैं। यह चलावयवता समावयवता को प्रदर्शित करते हैं तथा इस प्रकार की समावयवता उन यौगिकों में होती है, जिनमें कम-से-कम एक हाइड्रोजन होता है तथा एक स्थिति से दूसरे तक प्रोटॉन के स्थानांतरण के कारण उत्पन्न होती है इसे प्रोटोट्रॉफी कहते हैं।
प्रश्न 25.
संरूपण समावयवता किसे कहते हैं ?
उत्तर:
कार्बन-कार्बन एकल बंध के मध्य घूर्णन के कारण जो विभिन्न आकाशीय व्यवस्थाएँ उत्पन्न होती हैं वे संरूपी कहलाती हैं तथा संरूपियों से सम्बन्धित आण्विक ज्यामिति को संरूपण समावयवता कहते हैं।
![]()
प्रश्न 26.
बहुलीकरण अभिक्रिया को उदाहरण सहित समझाइये।
उत्तर:
वह रासायनिक अभिक्रिया जिसमें दो या दो से अधिक सरल इकाई जिन्हें एकलक कहते हैं। परस्पर संयोजन कर एक जटिल अणु का निर्माण करते हैं बहुलक कहलाते हैं तथा इस अभिक्रिया को बहुलीकरण कहते हैं।
उदाहरण – एथिलीन अणुओं के बहुलीकरण से पॉलीएथिलीन बनता है।
![]()
प्रश्न 27.
एल्कीन इलेक्ट्रॉन स्नेही योगात्मक अभिक्रियाएँ प्रदर्शित करती है, जबकि ऐरीन इलेक्ट्रॉनस्नेही प्रतिस्थापन अभिक्रियाएँ प्रदर्शित करती है। कारण स्पष्ट कीजिए।
उत्तर:
एल्कीन ढीले बँधे π – इलेक्ट्रॉनों के धनी स्रोत होते है, जिसके कारण ये इलेक्ट्रॉनस्नेही योगात्मक अभिक्रियाएँ प्रदर्शित करता है। ऐल्कीनों की इलेक्ट्रॉन स्नेही योगात्मक अभिक्रियाओं में ऊर्जा में अत्यधिक बदलाव आता है। जिसके कारण ये इलेक्ट्रॉन स्नेही प्रतिस्थापन अभिक्रियाओं की अपेक्षा ऊर्जात्मक रूप से अधिक प्रभावी होती है। एरीन में इलेक्ट्रॉन स्नेही योगात्मक अभिक्रिया के दौरान बेंजीन वलय की ऐरोमैटिक प्रकृति नष्ट हो जाती है जबकि इलेक्ट्रॉन स्नेही प्रतिस्थापन अभिक्रिया में यह स्थिर रहती है। ऐरीन की इलेक्ट्रॉन स्नेही प्रतिस्थापन अभिक्रियाएँ ऊर्जात्मक रूप से इलेक्ट्रॉन स्नेही योगात्मक अभिक्रियाओं की अपेक्षा अधिक प्रभावी होती है।
प्रश्न 28.
ज्यामितीय समावयवता की आवश्यक शर्ते क्या हैं ?
उत्तर:
ज्यामितीय समावयवता के लिये निम्नलिखित शर्ते आवश्यक हैं –
- इसमें कम-से-कम एक कार्बन-कार्बन द्विबंध होना चाहिए।
- द्विबंधित कार्बन परमाणु से जुड़े परमाणु या समूह भिन्न-भिन्न होने चाहिए।
प्रश्न 29.
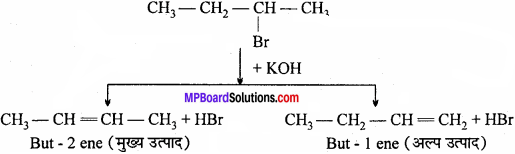
सेटजेफ नियम क्या है ? उदाहरण सहित समझाइये।
उत्तर:
यदि ऐल्किल हैलाइड में से हाइड्रोजन हैलाइड का विलोपन किया जाता है तो यह भिन्न-भिन्न प्रकार से हो सकता है तथा ऐल्कीन प्राप्त होता है। इस नियम के अनुसार उस ऐल्कीन के बनने की संभावना अधिक होगी, जिसमें द्विबंध से जुड़े कार्बन परमाणु अधिक ऐल्किलीकृत होते हैं। अर्थात् हाइड्रोजन का विलोपन उस कार्बन से होता है जहाँ हाइड्रोजन की संख्या कम होती है।
प्रश्न 30.
ऑक्टेन संख्या से आप क्या समझते हैं ?
उत्तर:
विभिन्न ईंधनों के तुलनात्मक अपस्फोटरोधी गुण को व्यक्त करने के लिए एडगर ने सन् 1927 में ऑक्टेन अंक शब्द प्रयुक्त किया, जिसके अनुसार किसी ईंधन की ऑक्टेन संख्या आवश्यकतानुसार आइसो ऑक्टेन के मिश्रण में उपस्थित होती है, जिसका किसी मानक (Standard) इंजन में अपस्फोटन दिये हुए ईंधन के अपस्फोटन के बराबर होता है, अर्थात् किसी ईंधन की ऑक्टेन संख्या, हेप्टेन तथा आइसो ऑक्टेन के मिश्रण में आइसो ऑक्टेन का प्रतिशत होती है।
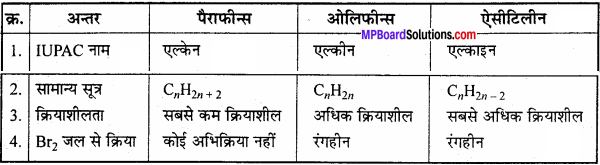
प्रश्न 31.
पैराफीन्स, ओलिफीन्स एवं ऐसीटिलीन की निम्न बिन्दुओं में तुलना कीजिए –
1. IUPAC नाम
2. सामान्य सूत्र
3. क्रियाशीलता
4. ब्रोमीन जल से क्रिया।
उत्तर:
हाइड्रोकार्बन लघु उत्तरीय प्रश्न
प्रश्न 1.
बेन्जीन, n – हेक्सेन तथा एथाइन को घटते हुए अम्लीय व्यवहार के क्रम में व्यवस्थित कीजिए और इस व्यवहार का कारण बताइए।
उत्तर:
दिये गये यौगिकों में कार्बन की संकरण अवस्था निम्न है –
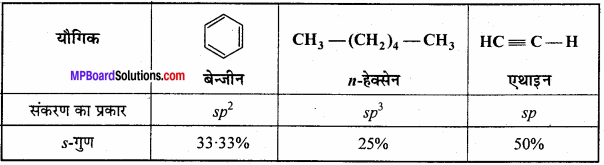
अम्लीय व्यवहार, कक्षक के S – गुण में वृद्धि के साथ-साथ बढ़ता है। अतः बेन्जीन, n-हेक्सेन तथा एथाइन के अम्लीय व्यवहार का घटता हुआ क्रम निम्न है –
ऐथाइन > बेन्जीन > n – हेक्सेन
प्रश्न 2.
किसी निकाय द्वारा ऐरोमैटिकता प्रदर्शित करने के लिए आवश्यक शर्ते क्या हैं ?
उत्तर:
किसी निकाय द्वारा ऐरोमैटिकता प्रदर्शित करने के लिए आवश्यक शर्ते निम्न हैं –
- अणु समतलीय होना चाहिए।
- अणु चक्रीय होना चाहिए जिसमें एकान्तर क्रम में एकल तथा द्विबंध होना चाहिए अर्थात् वलय में T – इलेक्ट्रॉनों का संपूर्ण विस्थानीकरण होना चाहिए।
- अणु के वलय (ring) में (4n + 2) π इलेक्ट्रॉन होने चाहिए। जहाँ n = 0,1,2,3 …….. (ह्यूकेल नियम)। यदि कोई अणु उपरोक्त में से किसी एक अथवा अधिक दशाओं को संतुष्ट नहीं कर पाता है, तो उसे अ-ऐरोमैटिक कहते हैं।
![]()
प्रश्न 3.
मध्यावयवता समावयवता क्या है ? उदाहरण सहित समझाइये।
उत्तर:
जब दो या दो से अधिक यौगिकों के अणुसूत्र समान हो और उनमें उपस्थित क्रियात्मक समूह भी समान हो लेकिन उनसे जुड़े एल्किल मूलक में भिन्नता हो तो इस प्रकार उत्पन्न समावयवता को मध्यावयवता कहते हैं।
उदाहरण –
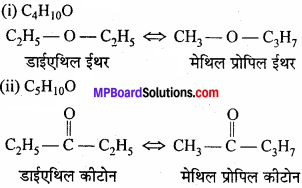
प्रश्न 4.
चलावयवता समावयवता क्या है ? उदाहरण सहित समझाइये।
उत्तर:
यह एक विशिष्ट प्रकार की क्रियात्मक समावयवता है, जिसमें दोनों समावयवयी साम्य अवस्था में होते हैं तथा सरलता से एक-दूसरे में परिवर्तित हो सकते हैं। इस प्रकार की समावयवता तब उत्पन्न होती है, जब हाइड्रोजन या कोई भी अन्य समूह द्विबंध या त्रिबंध के दोनों तरफ दोलन करता है।
यह दो प्रकार की होती है –
1. द्विक प्रणाली – इस प्रणाली में हाइड्रोजन का दोलन दो बहु-संयोजकीय परमाणुओं के बीच होता है।
उदाहरण – H – C = N – H – N – C
2. त्रिक प्रणाली – इस प्रणाली में हाइड्रोजन का दोलन तीन बहु-संयोजकीय परमाणुओं के बीच होता है।

इनॉल रूप इसे कीटो-इनॉल समावयवता भी कहते हैं।
प्रश्न 5.
न्यूमैन प्रक्षेपण सूत्र क्या है ?
उत्तर:
यदि दो कार्बन परमाणु के मध्य एकल बंध उपस्थित हो और दोनों कार्बन को एक वृत्त के रूप में दर्शाया जाये तथा इनसे जुड़े हाइड्रोजन को C – H बंध द्वारा उनके केन्द्र से जुड़ा हुआ दर्शाया जाये। यदि दोनों कार्बन एक-दूसरे के पीछे व्यवस्थित हो तो उनमें से केवल सामने वाला कार्बन दिखाई देता है तथा उससे जुड़े हुए तीनों हाइड्रोजन उसके केन्द्र से जुड़े दिखाई देते हैं तथा पीछे वाले कार्बन के हाइड्रोजन पहले कार्बन की परिधि पर जुड़े हुए दिखाई देते हैं।
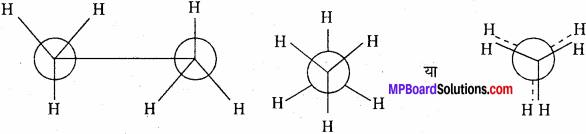
प्रश्न 6.
मार्कोनीकॉफ नियम क्या है ? उदाहरण सहित समझाइये।
उत्तर:
जब सममित हाइड्रोकार्बन पर असममित अभिकर्मक का योग होता है तो आक्रमणकारी समूह का एक भाग द्विबंध या त्रिबंध वाले एक कार्बन परमाणु पर तथा दूसरा भाग दूसरे कार्बन परमाणु पर जुड़ता है।
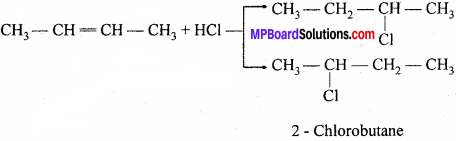
लेकिन जब असममित ऐल्कीन पर असममित अभिकर्मक का योग होता है तो सामान्यतः अभिक्रिया मार्कोनीकॉफ नियम के अनुसार होती है। इस नियम के अनुसार युग्म बंध पर जुड़ने वाले आक्रमणकारी समूह का ऋणात्मक भाग द्विबंध से जुड़े उस कार्बन परमाणु पर जुड़ता है जिस पर हाइड्रोजन की संख्या न्यूनतम होती है।
प्रश्न 7.
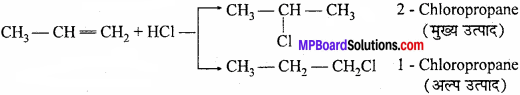
रेसेमिक मिश्रण को उदाहरण सहित समझाइये।
उत्तर:
दो प्रतिबिम्ब समावयवी की समान मात्राओं का मिश्रण ध्रुवण घूर्णकता नहीं दर्शाता क्योंकि मिश्रण में उपस्थित दोनों प्रतिबिम्ब समावयवी की ध्रुवण घूर्णकता बराबर किन्तु विपरीत दिशा में होती है तथा एक – दूसरे के कारण उत्पन्न ध्रुवण घूर्णकता को विनष्ट कर देती है। ऐसे मिश्रण को रेसेमिक मिश्रण कहते हैं तथा इसे dl या ± चिन्ह द्वारा दर्शाते हैं। उदाहरण – रेसेमिक लेक्टिक अम्ल – यह d तथा l रूप का समअणुक मिश्रण है। इसमें 50% d रूप तथा 50% l रूप होता है। यह रूप ध्रुवण अघूर्णक होता है तथा इसे d तथा l रूप में वियोजित किया जा सकता है। इसे dl या ± द्वारा दर्शाते हैं।
प्रश्न 8.
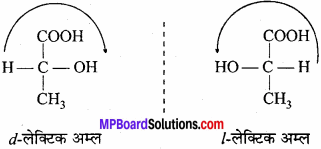
ऐल्केन की प्रतिस्थापन अभिक्रिया को उदाहरण सहित समझाइये।
उत्तर:
वह अभिक्रिया जिसमें किसी यौगिक में उपस्थित परमाणु किसी अन्य परमाणु या मूलक से इस प्रकार प्रतिस्थापित होता है कि यौगिक की आंतरिक संरचना में कोई परिवर्तन नहीं आता प्रतिस्थापन अभिक्रिया कहलाती है। ऐल्केन में होने वाली हैलोजनीकरण, नाइट्रीकरण, सल्फोनीकरण अभिक्रिया इसके उदाहरण हैं। हैलोजनीकरण अभिक्रिया – ऐल्केन की अभिक्रिया क्लोरीन के साथ सूर्य प्रकाश की उपस्थिति में कराने पर ऐल्केन में उपस्थित हाइड्रोजन का प्रतिस्थापन क्लोरीन द्वारा होता है तथा क्रमशः मोनो, डाई, ट्राई तथा टेट्रा हैलोएल्केन का मिश्रण प्राप्त होता है।
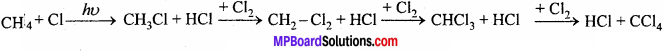
प्रश्न 9.
B.H.C. क्या है ? इसका उपयोग बताइये।
उत्तर:
बेंजीन की अभिक्रिया सूर्य प्रकाश अथवा पराबैंगनी प्रकाश की उपस्थिति में क्लोरीन से कराने पर बेंजीन हेक्साक्लोराइड प्राप्त होता है।
यह आठ त्रिविम समावयवयी रूपों में मिलता है। लेकिन इसके केवल चार समावयवयी रूप α β γ या δ रूप को शुद्ध अवस्था में प्राप्त किया जा सकता है। इसके विभिन्न समावयवयी रूप हाइड्रोजन तथा क्लोरीन की विभिन्न व्यवस्थाओं के कारण उत्पन्न होते हैं। इसका γ समावयवयी रूप सबसे अधिक स्थायी तथा प्रबल कीटनाशी है। इसको लिण्डेन या गैमेक्सेन या 666 के नाम से भी जाना जाता है। इसका उपयोग कीटाणुनाशक के रूप में होता है।
![]()
प्रश्न 10.
निम्नलिखित परिवर्तन कैसे करोगे केवल समीकरण दीजिए –
- मेथेन से एथेन
- एथेन से मेथेन
- ऐसीटिलीन से बेंजीन।
उत्तर:
1. मेथेन से एथेन –
2. एथेन से मेथेन –
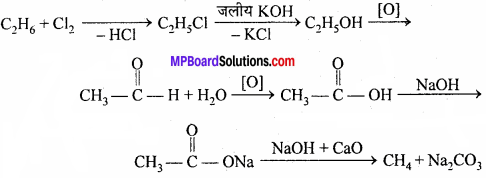
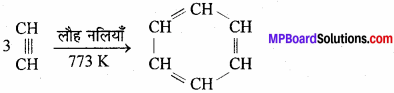
3. ऐसीटिलीन से बेंजीन –
प्रश्न 11.
कैसे प्राप्त करोगे (केवल समीकरण दीजिए) –
- बेंजीन से B.H.C.
- बेंजीन से ऐसीटोफिनोन
- क्लोरोएथीन से पी.वी.सी.
- टेट्राफ्लोरो एथीन से टेफ्लॉन।
उत्तर:
1. बेंजीन से B.H.C –
![]()
2. बेंजीन से ऐसीटोफिनोन –

3. क्लोरोएथीन से –

4. टेट्राफ्लोरो एथीन से टेफ्लॉन
![]()
प्रश्न 12.
ज्यामितीय समावयवता किस प्रकार के यौगिकों में पायी जाती है ? उदाहरण सहित समझाइये।
उत्तर:
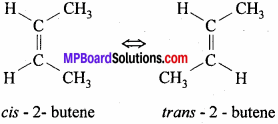
यह एक प्रकार की त्रिविम समावयवता है। जो युग्म बंध युक्त ऐसे यौगिकों द्वारा प्रदर्शित की जाती है, जिनमें युग्म बंधित कार्बन परमाणु से जुड़े दो परमाणु या समूह भिन्न-भिन्न प्रकार के हो सकते हैं। जब समान परमाणु या समूह द्विबंध के एक ओर स्थित होते हैं तो प्राप्त यौगिक समपक्ष समावयवयी कहलाता है तथा जब विपरीत परमाणु या समूह द्विबंध के एक ओर स्थित हो तो प्राप्त यौगिक विपक्ष समावयवयी कहलाता है। इसलिये इसे समपक्ष-विपक्ष समावयवता भी कहते हैं।

उदाहरण – 2 – butene
प्रश्न 13.
ह्यूकेल का नियम क्या है ?
उत्तर:
ह्यूकेल ने अनेक ऐरोमैटिक यौगिकों का अध्ययन करने के पश्चात् एक नियम प्रतिपादित किया जिसे ह्यूकेल का नियम कहते हैं। इस नियम के अनुसार वे सभी समतलीय चक्रीय यौगिक ऐरोमैटिक गुण प्रदर्शित करते हैं। जिनके चक्र में (4n + 2) π इलेक्ट्रॉन होते हैं, यहाँ n पूर्णांक है जिसका मान 0, 1, 2 ………. होता है। अत: जिन चक्रीय यौगिक में 6(n = 1), 10 (n = 2), 14(n=3) इलेक्ट्रॉन होते हैं, उनमें ऐरोमैटिक गुण होता – है। ऐरोमैटिक यौगिक दो प्रकार के होते हैं –
1. बेंजीनोइड्स – वे यौगिक जो एक या अधिक बेंजीन वलय युक्त होते हैं, बेंजीनोइड्स कहलाते हैं।

2. नॉन – बेन्जीनोइड्स – ऐसे यौगिक जिनमें बेंजीन रिंग नहीं होती है।

प्रश्न 14.
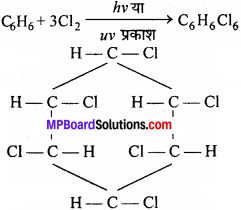
ऐल्कीन सरलता से योगात्मक अभिक्रिया प्रदर्शित करता है, क्यों ?
उत्तर:
ऐल्कीन एक असंतृप्त हाइड्रोकार्बन है। इसमें कार्बन – कार्बन के बीच द्विबंध होता है तथा इस द्विबंध में एक σ बंध एक π बंध होता है। बंध – बंध की तुलना में दुर्बल होता है। इस π बंध की उपस्थिति के कारण एल्कीन सरलता से योगात्मक अभिक्रिया दर्शाता है। इस योगात्मक अभिक्रिया के दौरान एक π बंध टूटता है तो दो नये σ बंध का निर्माण होता है।
CH2 = CH2 + HCl → CH3 – CH2Cl
![]()
प्रश्न 15.
फ्रीडल क्राफ्ट्स अभिक्रिया को समीकरण सहित दर्शाइये।
उत्तर:
एल्किलीकरण:
बेंजीन की अभिक्रिया निर्जल AlCl3 की उपस्थिति में CH3Cl के साथ कराने पर टॉलुईन प्राप्त होता है। इस अभिक्रिया के दौरान बेंजीन में से हाइड्रोजन का प्रतिस्थापन एल्किल समूह द्वारा होता है इसलिये इसे एल्किलीकरण कहते हैं।

एसिलीकरण – बेंजीन की अभिक्रिया निर्जल AlCl3 की उपस्थिति में एसीटिल क्लोराइड
के साथ कराने पर एसीटोफिनोन प्राप्त होता है। इस अभिक्रिया के दौरान बेंजीन में से हाइड्रोजन का प्रतिस्थापन एसीटिल या एसिल समूह द्वारा होता है। इसलिये इसे एसिटलीकरण या एसिलीकरण अभिक्रिया कहते हैं।

प्रश्न 16.
ज्यामितीय समावयवियों के नामकरण हेतु E व z संकेत क्या है ?
उत्तर:
जब द्विबंधित कार्बन परमाणु पर सभी चारों समूह अलग – अलग हों तो ज्यामितीय समावयवियों को E व Z संकेत से दर्शाते हैं। ये निम्न अनुक्रम नियम पर आधारित हैं –
नियम I:
सभी परमाणु और समूह जो द्विबंधित कार्बन परमाणु से जुड़े होते हैं। उनके प्रथम परमाणु के परमाणु क्रमांक के बढ़ते क्रम के आधार पर उनकी प्राथमिकता निर्भर करते हैं। कम परमाणु क्रमांक वाले परमाणु या समूह को निम्नतम प्राथमिकता देते हैं तथा अधिक परमाणु क्रमांक वाले परमाणु या समूह को उच्चतम प्राथमिकता देते हैं । यदि इन समूह के प्रथम परमाणु समान हों तो द्वितीय परमाणु अथवा तृतीय परमाणु के परमाणु क्रमांक द्वारा प्राथमिकता का अनुक्रम निर्धारित करते हैं।
नियम II:
जब द्विबंध से बँधे दोनों कार्बन परमाणु पर उच्च प्राथमिकता वाले परमाणु या समूह विपरीत ओर एक ही दिशा में हो तो इस विन्यास को E रूप से दर्शाते हैं। जब यदि द्विबंध से बँधे दोनों कार्बन परमाणु पर उच्च प्राथमिकता वाले परमाणु या समूह एक ही दिशा में हो तो इस विन्यास को Z रूप से दर्शाते हैं।
उदाहरण –

प्रश्न 17.
डाइईन्स किसे कहते हैं ? डाइईन्स कितने प्रकार के होते हैं ? उदाहरण सहित समझाइये।
उत्तर:
डाइईन्स असंतृप्त हाइड्रोकार्बन है, इनमें कार्बन श्रृंखला में कार्बन – कार्बन के मध्य दो द्विबंध होते हैं तथा द्विबंधों की सापेक्षिक स्थिति के आधार पर डाइईन्स तीन प्रकार के होते हैं –
1. विलगित डाइईन्स:
ऐसे डाइईन्स जिसमें दो द्विबंध परस्पर एक से अधिक एकल बंधों द्वारा अलग होते हैं।
CH2 = CH – CH2 – CH = CH2
2. संयुग्मित डाइईन्स – ऐसे डाइईन्स में दो द्विबंध संयुग्मित या एकान्तर स्थिति पर होते हैं।
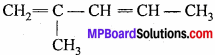
3. संचयी डाइईन्स – इन डाइईन्स में दो द्विबंध समीपस्थ स्थिति पर होते हैं।
CH2 = C = CH – CH3
CH3 – CH = C = CH2
प्रश्न 18.
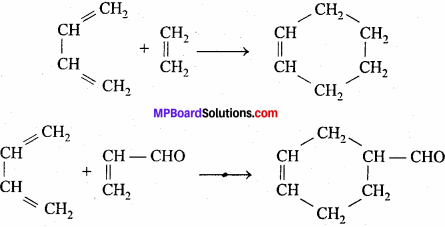
डील्स एल्डर अभिक्रिया को समीकरण सहित लिखिए।
उत्तर:
जब संयुग्मित डाइईन्स को किसी एल्कीन या प्रतिस्थापित एल्कीन के साथ गर्म करते हैं तो एक छः सदस्यीय चक्रीय यौगिक बनता है इसलिये इस अभिक्रिया को चक्रीय संकलन अभिक्रिया भी कहते हैं। इसमें एक 47 इलेक्ट्रॉन निकाय से जुड़ता है। इस तरह की अभिक्रिया को डील्स एल्डर अभिक्रिया कहते हैं।
प्रश्न 19.
लिण्डलार उत्प्रेरक क्या है ? तथा इसके उपयोग लिखिए।
उत्तर:
बेरियम सल्फेट या कैल्सियम कार्बोनेट पर निक्षेपित पैलेडियम उत्प्रेरक का मिश्रण लिण्डलार उत्प्रेरक कहलाता है। यहाँ सल्फर या क्विनोलीन उत्प्रेरक विष का कार्य करता है और केवल एल्कीन अवस्था तक ही एल्काइन का अपचयन करता है।
उपयोग – एल्काइन का अपचयन हाइड्रोजन द्वारा लिण्डलार उत्प्रेरक की उपस्थिति में कराने पर एल्कीन प्राप्त होता है। यह उत्प्रेरक आगे एल्कीन को एल्केन में अपचयित नहीं होने देता।
![]()
प्रश्न 20.
बेंजीन की संरचना के लिये कैकुले सूत्र के पक्ष में चार प्रमाण दीजिए।
उत्तर:
बेंजीन की संरचना के लिये कैकुले सूत्र के पक्ष में प्रमाण –
1. बेंजीन तीन अणु हाइड्रोजन के साथ संयोग कर चक्रीय यौगिक साइक्लोहेक्सेन बनाता है, जिससे बेंजीन में तीन युग्म बंध की पुष्टि होती है।

2. बेंजीन तीन अणु क्लोरीन से संयोग कर B.H.C. बनाता है। अतः यह भी तीन युग्म बंध की पुष्टि करता है।
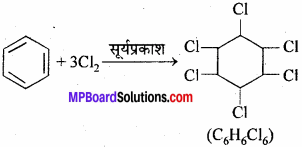
3. बेंजीन ओजोन के साथ संयोग कर ट्राइ ओजोनाइड बनाता है जो जल अपघटित होकर ग्लाईऑक्सेल के तीन अणु बनाता है।
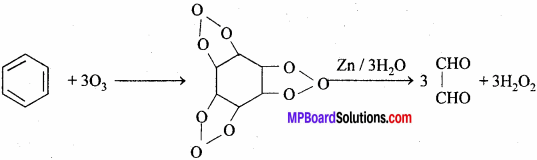
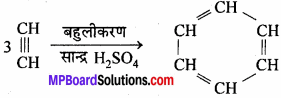
4. एसीटिलीन के तीन अणु बहुलीकरण के द्वारा बेंजीन का निर्माण करते हैं। ..
प्रश्न 21.
कारण दीजिए –
1. शाखायुक्त यौगिकों के क्वथनांक सीधी श्रृंखला युक्त यौगिकों की अपेक्षा कम होते हैं, क्यों ?
2. विषम संख्या कार्बन परमाणु वाले यौगिक के गलनांक सम संख्या कार्बन परमाणु वाले यौगिकों से कम होते हैं, क्यों?
उत्तर:
1. रेखीय शृंखला वाले कार्बनिक यौगिकों का पृष्ठीय क्षेत्रफल अधिक होता है और इनमें अंतरअणुक आकर्षण बल अधिक होता है जबकि कार्बन परमाणु की श्रृंखला में शाखायुक्त हो जाने पर अणु में स्थित विभिन्न परमाणु पास-पास आ जाते हैं, जिससे उनके बीच अंतर-अणुक आकर्षण बल कम होता है इसलिये श्रृंखला वाले यौगिकों का क्वथनांक शाखायुक्त यौगिकों से अधिक होता है।
2. कार्बन परमाणु की विषम संख्या युक्त ऐल्केन कार्बन श्रृंखला के सिरों पर स्थित कार्बन परमाणु समान पक्ष में होते हैं। जबकि कार्बन परमाणु की सम संख्या वाले ऐल्केन में कार्बन शृंखला के सिरों पर स्थित कार्बन विपरीत पक्ष में होते हैं। सम संख्या वाले यौगिकों के विषम कार्बन संख्या वाले यौगिकों की तुलना में पैकिंग अधिक सघन होती है। इसलिए सम कार्बन संख्या वाले यौगिकों के क्वथनांक अधिक होते हैं।
![]()
प्रश्न 22.
निम्नलिखित पर टिप्पणी लिखिए –
- सबात्ये और सेण्डरेन्स अभिक्रिया
- बुर्दज अभिक्रिया
- इयमा अभिक्रिया
- स्वार्ट अभिक्रिया।
उत्तर:
1. सबात्ये और सेण्डरेन्स अभिक्रिया – ऐल्कीन की अभिक्रिया Ni या Pt की उपस्थिति में हाइड्रोजन के साथ कराने पर हाइड्रोजनीकरण के पश्चात् ऐल्केन प्राप्त होता है।
![]()
2. बुर्दज अभिक्रिया – दो अणु ऐल्किल हैलाइड की अभिक्रिया सोडियम के साथ शुष्क ईथर की उपस्थिति में कराने पर ऐल्केन प्राप्त होता है। इस प्रकार प्राप्त ऐल्केन में ऐल्किल हैलाइड की तुलना में दो गुना ज्यादा कार्बन होते हैं।
![]()
3. ड्यूमा अभिक्रिया – मोनोकार्बोक्सिलिक अम्ल के सोडियम लवण की अभिक्रिया सोडालाइम के साथ कराने पर विकार्बोक्सीकरण के पश्चात् एल्केन प्राप्त होता है।
![]()
4. स्वार्ट अभिक्रिया – जब एल्किल हैलाइड की अभिक्रिया मरक्यूरिक फ्लोराइड के साथ कराने पर फ्लोरो एल्केन प्राप्त होता है। इस अभिक्रिया के दौरान एल्किल हैलाइड के हैलोजन का प्रतिस्थापन फ्लोरीन द्वारा होता है।
2C2H5 – I + HgF2 → 2CH3 → 2C2H5 + F + HgI2
प्रश्न 23.
कोल्बे की वैद्युत अपघटन अभिक्रिया को समीकरण सहित लिखिए।
उत्तर:
मोनो कार्बोक्सिलिक अम्ल के सोडियम या पोटैशियम लवण के सान्द्र जलीय विलयन का वैद्युत अपघटन करने पर एनोड पर एल्केन प्राप्त होता है।
![]()
![]()
एनोड पर – एसीटेट आयन इलेक्ट्रॉन त्यागकर उदासीन हो जाता है और विघटित होकर एल्केन देता है।
2CH3COO– – 2e– → 2CH3 COO → C2H6 + 2CO2
कैथोड पर – हाइड्रोजन आयन इलेक्ट्रॉन ग्रहण कर हाइड्रोजन देता है।
2Na+ + 2HOH + 2e– → 2NaOH + H2
प्रश्न 24.
निम्नलिखित अभिक्रियाओं के केवल समीकरण दीजिए –
- कैल्सियम कार्बाइड की जल से।
- एथिलीन पर ब्रोमीन जल की अभिक्रिया।
- एथिलीन को क्षारीय KMnO4के साथ गर्म करने पर।
- बेंजीन को सान्द्र HNOJ तथा सान्द्र H2SO, के साथ गर्म करने पर।
- बेंजीन को मेथिल क्लोराइड के साथ निर्जल AICI, की उपस्थिति में गर्म करने पर।
उत्तर:
1. कैल्सियम कार्बाइड की जल के साथ अभिक्रिया –
CaC2 + 2HOH → CH = CH + Ca(OH)2
2. एथिलीन पर ब्रोमीन जल की अभिक्रिया –
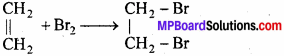
3. एथिलीन को क्षारीय KMnO, के साथ गर्म करने पर

4. बेंजीन को सान्द्र HNOJ तथा सान्द्र H,SO, के साथ गर्म करने पर –

5. बेंजीन को CHICI के साथ निर्जल AICI की उपस्थिति में गर्म करने पर

प्रश्न 25.
निम्नलिखित को कैसे प्राप्त करोगे
- एसीटिलीन से एसिटैल्डिहाइड
- एथिलीन से मस्टर्ड गैस
- ग्रिगनार्ड अभिकर्मक से एथेन
- एसीटिलीन से क्यूप्रस एसीटिलाइड
- ऐल्युमिनियम कार्बाइड से मेथेन।
उत्तर:
1. एसीटिलीन से एसिटैल्डिहाइड –
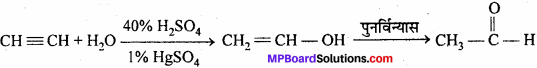
2. एथिलीन से मस्टर्ड गैस –
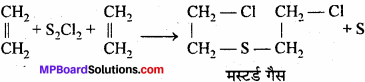
3. ग्रिगनार्ड अभिकर्मक से एथेन –

4. एसीटिलीन से क्यूप्रस एसीटिलाइड –
CH ≡ CH + Cu2Cl2 + 2NH4OH D Cu – C ≡ C – Cu + 2NH4Cl + 2H2O
5. ऐल्युमिनियम कार्बाइड से मेथेन –
Al4C3 + 12H2 O → 3CH4 + 4Al(OH)2
प्रश्न 26.
किसी प्राथमिक ऐल्किल हैलाइड की वु अभिक्रिया कराने पर एकमात्र उत्पाद के रूप में C8H18 प्राप्त होता है। इस ऐल्केन का मोनोब्रोमीकरण करने पर तृतीयक ब्रोमाइड का एकल समावयव प्राप्त होता है। ऐल्केन तथा तृतीयक ब्रोमाइड की पहचान लिखिए।
उत्तर:
चूँकि ऐल्केन C8H18 मोनोब्रोमीकरण के पश्चात् तृतीयक ब्रोमाइड का एक समावयव बनाता है अतः ऐल्केन में तृतीयक हाइड्रोजन उपस्थित होनी चाहिए। यह तभी सम्भव है जबकि प्राथमिक ऐल्किल हैलाइड (जो वु अभिक्रिया में भाग लेता है) के पास तृतीयक हाइड्रोजन हो।

प्रश्न 27.
2 – मेथिल प्रोपेन के मोनो क्लोरीनीकरण में बनने वाले मध्यवर्ती हाइड्रोकार्बन मूलकों को लिखिए। इनमें से कौन-सा अधिक स्थायी होगा। कारण भी दीजिए।
उत्तर:
2-मेथिल प्रोपेन निम्न दो प्रकार के मूलक देता है, जो निम्न है –
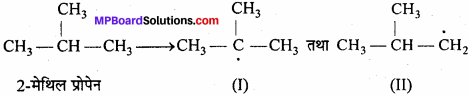
मूलक (I) अधिक स्थायी है क्योंकि यह 3° मुक्त मूलक है तथा नौ अति संयुग्मित संरचनाओं को स्थायी करता है (क्योंकि इसमें 9a -हाइड्रोजन है।)
मूलक (II) कम स्थायी है क्योंकि यह 1° मुक्त मूलक है तथा यह केवल एक अति संयुग्मित संरचना को स्थायी करता है। (क्योंकि इसमें केवल 1a- हाइड्रोजन है।)
![]()
प्रश्न 28.
विहाइड्रोहैलोजनीकरण तथा विहैलोजनीकरण अभिक्रिया को उदाहरण सहित समझाइये।
उत्तर:
विहाइड्रोहैलोजनीकरण – किसी कार्बनिक यौगिक में हाइड्रोजन हैलाइड के अणु का विलोपन विहाइड्रोहैलोजनीकरण कहलाता है। इस अभिक्रिया के दौरान β स्थिति से हाइड्रोजन का विलोपन होता है। इसलिये इसे β विलोपन अभिक्रिया भी कहते हैं।

उदाहरण – नॉर्मल प्रोपिल क्लोराइड को एल्कोहॉलिक KOH के साथ गर्म करने पर एल्कीन प्राप्त होता है।
CH3 – CH2 – CH2 – Cl + KOH → CH3 – CH = CH2 + KCl + H2O
विहैलोजनीकरण – बिस डाइहैलाइड को Zn चूर्ण के साथ मेथिल एल्कोहॉल की उपस्थिति में गर्म करने पर एल्कीन प्राप्त होता है, इस अभिक्रिया के दौरान केवल हैलोजन का विलोपन होता है इसलिए इसे विहैलोजनीकरण अभिक्रिया कहते हैं।

प्रश्न 29.
क्या होता है जब
- सोडियम एसीटेट को सोडालाइम के साथ गर्म करने पर।
- 2 – प्रोपेनॉल को एलुमिना के साथ 300°C ताप पर गर्म करने पर।
- एसीटिलीन को अमोनियामय AgNO3 के विलयन में प्रवाहित करने पर।
- एथिल आयोडाइड को सोडियम के साथ गर्म करने पर।
- एथिलीन पर हाइपोक्लोरस अम्ल की अभिक्रिया कराने पर।
उत्तर:
1. सोडियम एसीटेट को सोडालाइम के साथ गर्म करने पर –
![]()
2. 2-प्रोपेनॉल को एलुमिना के साथ 300°C ताप पर गर्म करने पर –
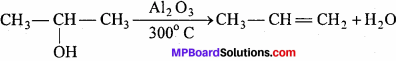
3. एसीटिलीन को अमोनियामय AgNOJ के साथ गर्म करने पर –
CH ≡ CH + 2AgNO3 + 2NH4OH → Ag – C ≡ C – Ag + 2NH4NO3 + 2H2O
4. एथिल आयोडाइड को सोडियम के साथ गर्म करने पर –
![]()
5. एथिलीन पर हाइपोक्लोरस अम्ल की अभिक्रिया कराने पर –

प्रश्न 30.
निम्नलिखित पर टिप्पणी लिखिए –
1. हाइड्रोबोरोनीकरण
2. एपॉक्सीकरण।
उत्तर:
1. हाइड्रोबोरोनीकरण – एल्कीन पर जब डाइबोरेन से अभिक्रिया करायी जाती है तब एल्कीन के द्विबंध पर योगात्मक क्रिया होती है एवं ट्राइऐल्किल बोरेन बनता है, जो जल अपघटन पर एल्कोहॉल देता है यह हाइड्रोबोरोनीकरण अभिक्रिया कहलाती है।

2. एपॉक्सीकरण – एल्कीन ऑक्साइड को एपॉक्साइड कहते हैं। एल्कीन के ऑक्सीकरण से एपॉक्साइड बनने की क्रिया एपॉक्सीकरण कहलाती है।
उदाहरण – निम्नतर एल्कीन 200 – 400°C ताप पर सिल्वर उत्प्रेरक की उपस्थिति में ऑक्सीजन से संयोग करके एपॉक्साइड बनते हैं।
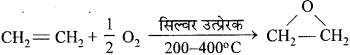
प्रश्न 31.
वुज अभिक्रिया को विषम कार्बन संख्या वाले ऐल्केन बनाने के लिये क्यों उपयुक्त नहीं माना जाता है ?
उत्तर:
एल्किल हैलाइड के दो अणु सोडियम के साथ शुष्क ईथर की उपस्थिति में गर्म करने पर ऐल्केन प्राप्त होता है।
![]()
इस अभिक्रिया द्वारा विषम कार्बन संख्या वाले ऐल्केन का निर्माण नहीं किया जा सकता है। क्योंकि इसके लिये दो अलग-अलग एल्किल हैलाइड को सोडियम के साथ गर्म करने पर ऐल्केनों का मिश्रण प्राप्त होता है जिन्हें पृथक् करना बहुत कठिन होता है। उदाहरण के लिये यदि मेथिल ब्रोमाइड तथा एथिल ब्रोमाइड को शुष्क ईथर की उपस्थिति में सोडियम के साथ गर्म करने पर एथेन, प्रोपेन तथा ब्यूटेन का मिश्रण प्राप्त होता है और इसमें से प्रोपेन को पृथक् करना अत्यन्त कठिन होता है।
![]()
प्रश्न 32.
HI, HBr तथा HCl की प्रोपीन के साथ क्रिया में बना मध्यवर्ती कार्बधनायन समान रहता है। HCl, HBr तथा Hl की आबंध ऊर्जाएँ क्रमशः 430.5 kJmol– 363.7 kJmol– तथा 296.8 kJmol– होती है। इन हैलोजन अम्लों की क्रियाशीलता का क्रम क्या होगा?
उत्तर:
हैलोजन अम्लों का ऐल्कीन के साथ योग एक इलेक्ट्रॉन स्नेही योगात्मक अभिक्रिया है।

चूँकि प्रथम पद मंद है अतः यह दर निर्धारक पद है। इस पद की दर, प्रोटॉन की उपलब्धता पर निर्भर करती है। जो पुनः H – X अणुओं की आबंध वियोजन ऊर्जा पर निर्भर करती है। H – X अणु की आबंध वियोजन ऊर्जा जितनी कम होती है, हैलोजन अम्ल की क्रियाशीलता उतनी ही अधिक होती है। अतः हैलोजन अम्लों की क्रियाशीलता का घटता हुआ क्रम निम्न है
HI(296.8kJ) > HBr(363.7kJ) > HCl(430.5kJ)
![]()
प्रश्न 33.
भंजन से क्या समझते हैं ? भंजन तथा इसके उपयोग पर टिप्पणी लिखिए।
उत्तर:
उच्च ताप के द्वारा या उत्प्रेरक की उपस्थिति में उच्चतर और जटिल हाइड्रोकार्बन का सरल हाइड्रोकार्बन में होने वाला अपघटन भंजन कहलाता है। दूसरे शब्दों में, कम वाष्पशील तथा उच्च हाइड्रोकार्बन का अधिक वाष्पशील तथा निम्न हाइड्रोकार्बन में तापीय अपघटन भंजन कहलाता है।
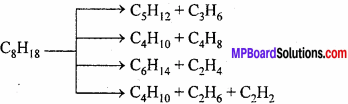
भंजन दो प्रकार का होता है –
1. ताप भंजन – जब भंजन उच्च ताप व दाब की परिस्थिति में उत्प्रेरक की अनुपस्थिति में कराया जाता है, तो इसे तापीय भंजन कहते हैं।
2. उत्प्रेरक भंजन – जब उत्प्रेरक की उपस्थिति में भंजन कराया जाता है, तो उसे उत्प्रेरक भंजन कहते हैं। उत्प्रेरक की उपस्थिति में भंजन तापीय भंजन की तुलना में कम ताप तथा कम दाब पर कराया जाता है।
उपयोग –
- मिट्टी के तेल से गैस बनाना।
- पेट्रोल के भंजन से पेट्रोलियम गैस बनाना।
प्रश्न 34.
एक हाइड्रोकार्बन A वाष्प घनत्व (14) बेयर अभिकर्मक को रंगहीन कर निम्नानुसार रासायनिक क्रिया करता है –
![]()
प्राप्त उत्पादों A, B, C और D के नाम और सूत्र लिखिये।
उत्तर:

(A) एथीलीन, (B) 1, 2 डाई ब्रोमो एथेन या एथीलीन ब्रोमाइड ,(C) एसीटिलीन, (D) एसीटेल्डिहाइड।
हाइड्रोकार्बन दीर्घ उत्तरीय प्रश्न
प्रश्न 1.
एल्कीन बनाने की प्रयोगशाला विधि का चित्र सहित वर्णन कीजिए।
उत्तर:
प्राथमिक एल्कोहॉल को सान्द्र H2SO4 के आधिक्य के साथ 170°C ताप पर गर्म करने पर एल्कोहॉल में से एक जल का अणु निकल जाता है और निर्जलीकरण के पश्चात् एल्कीन प्राप्त होता है।
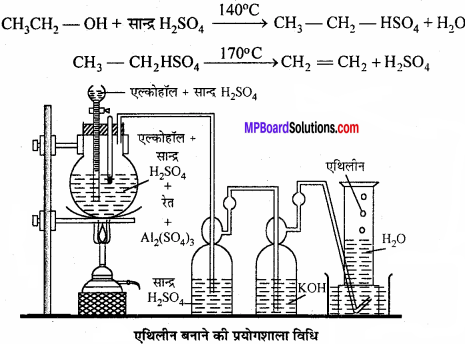
एक गोल पेंदी वाले फ्लास्क में एल्कोहॉल तथा सान्द्र H2SO लेते हैं। इस मिश्रण में निर्जल Al(SOA)3 तथा रेत मिलाते हैं। AICSO), तथा रेत का मिश्रण झाग उत्पन्न होने नहीं देता तथा अभिक्रिया 140°C ताप पर ही सम्पन्न हो जाती है। आसवन फ्लास्क में या गोल पेंदी वाले फ्लास्क में एक थर्मामीटर, बिन्दुपाती कीप तथा निकास नली लगाते हैं। निकास नली का दूसरा सिरा दो वाष्प बोतलों से जुड़ा रहता है।
जिसमें सान्द्र H SoA तथा KOH भरा रहता है। बिन्दुपाती कीप की सहायता से एल्कोहॉल तथा सान्द्र H2SOA के मिश्रण को गिराते हैं। इसे बालू उष्मक पर 150°C ताप पर गर्म करते हैं । बनने वाली एथिलीन गैस में SO, तथा CO, की अशुद्धि भी होती है जो क्रमशः H,SO, तथा KOH में अवशोषित हो जाती है और शुद्ध एथिलीन गैस को गैस जार में जल के ऊपर एकत्रित कर लेते हैं।
![]()
प्रश्न 2.
एसीटिलीन बनाने की प्रयोगशाला विधि का चित्र सहित वर्णन कीजिए।
अथवा
एसीटिलीन बनाने की प्रयोगशाला विधि का वर्णन निम्नांकित बिन्दुओं के आधार पर कीजिए
- विधि एवं रासायनिक समीकरण
- नामांकित चित्र।
उत्तर:
प्रयोगशाला में एसीटिलीन गैस को CaC2पर जल की अभिक्रिया द्वारा बनाया जाता है। इस विधि से प्राप्त एसीटिलीन में NH3 तथा PH3 की अशुद्धि होती है जिन्हें दूर करने के लिये इसे अम्लीय CuSO4 में प्रवाहित करते हैं।
CaC2 + 2H2O → CH == CH + Ca(OH)2
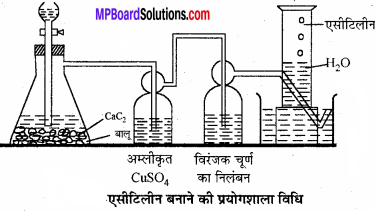
एक कोनिकल फ्लास्क में थोड़ी – सी रेत लेकर उसके ऊपर CaC2 के टुकड़े रखते हैं तथा फ्लास्क में उपस्थित वायु को तेल गैस प्रवाहित कर विस्थापित कर देते हैं। कोनिकल फ्लास्क में बिन्दुपाती कीप तथा निकास नली लगी होती है। बिन्दुपाती कीप की सहायता से CaC2 पर धीरे-धीरे H2O की बूंदें डालते हैं जिससे एसीटिलीन गैस प्राप्त होती है। जिसे अम्लीय CuSO4 विलयन में प्रवाहित कर – एसीटिलीन विरंजक चूर्ण के निलंबन में प्रवाहित करते ram हैं तथा एसीटिलीन गैस को गैस जार में जल के ऊपर एकत्रित कर लेते हैं।
सावधानी:
- प्रयोग के पूर्व बालू फ्लास्क की वायु को तेल गैस द्वारा विस्थापित कर देते हैं क्योंकि एसीटिलीन अम्लीकृत विरंजक चूर्ण Cuson का निलंबन वायु के साथ विस्फोटक मिश्रण बनाती है।
- CaC2 के ऊपर धीरे-धीरे जल डाला जाता है क्योंकि अभिक्रिया बहुत तीव्र गति से होती है।
- फ्लास्क की तली में पहले रेत रखकर CaC2 के टुकड़ों को रखा जाता है क्योंकि अभिक्रिया में बहुत अधिक मात्रा में ऊष्मा प्राप्त होती है।
प्रश्न 3.
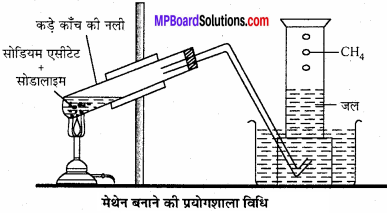
मेथेन बनाने की प्रयोगशाला विधि का सचित्र वर्णन कीजिए।
उत्तर:
वसीय अम्लों के सोडियम लवणों को सोडा लाइम के साथ 630°K ताप पर गर्म करने पर एल्केन प्राप्त होता है। कॉस्टिक सोडा NaOH तथा अनबुझा चूना Cao के मिश्रण को सोडा लाइम कहते हैं। यहाँ अभिक्रिया में केवल NaOH भाग लेता है Cao, NaOH को शुष्क रखता है और NaOH की तीव्रता को कम करता है जिससे काँच पर अभिक्रिया नहीं हो पाती।
![]()
एक कठोर काँच की नली में कडे काँच की नली सोडियम एसीटेट व सोडालाइम का मिश्रण लेते हैं तथा कॉर्क की सहायता साड से इसमें निकास नली लगाते हैं। जिसका सोडालाइम दूसरा सिरा जल से भरे गैस जार में लगा रहता है। सोडियम एसीटेट व सोडा लाइम के मिश्रण को परखनली में बुन्सन बर्नर पर गर्म करते हैं तथा बनने वाली मेथेन गैस को जल से भरे गैस जार में जल के ऊपर एकत्रित कर लेते हैं।
प्रश्न 4.
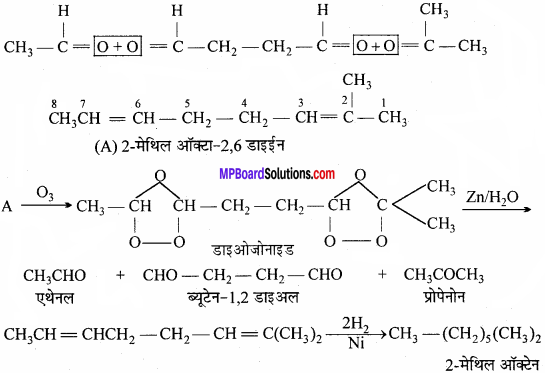
एक असंतृप्त हाइड्रोकार्बन ‘A’ दो अणु H, को जोड़ता है तथा अपचयित ओजोनीकरण के पश्चात् ब्यूटेन-1,4 डाइअल, एथेनल तथा प्रोपेनोन देता है। यौगिक ‘A’ की संरचना तथा IUPAC नाम लिखिए। प्रयुक्त अभिक्रियाओं को समझाइए।
उत्तर:
हाइड्रोकार्बन ‘A’ में दो अणु H2 का योग हो सकता है। अतः ‘A’ एल्केन, डाइईन या ऐल्काइन होना चाहिए। अपचयित ओजोनीकरण के पश्चात् ‘A’ तीन स्पीशीज देता है जिनमें से एक डाइऐल्डिहाइड है। इसका अर्थ है कि अणु दोनों सिरों से टूटता है। अतः ‘A’ में दो द्विआबंध होने चाहिए। यह निम्नलिखित तीन स्पीशीज देता है।
![]()
अतः यौगिक ‘A’ की संरचना निम्न है –
प्रश्न 5.
एसीटिलीन की अम्लीय प्रकृति को उदाहरण सहित समझाइये।
उत्तर:
ऐसे एल्काइन जिनके अणु के अंतिम छोर में = बंध होता है वे दुर्बल अम्लीय प्रकृति दर्शाते हैं। इनकी अम्लीय प्रकृति को संकरण के आधार पर समझाया जा सकता है। ऽ कक्षक में उपस्थित इलेक्ट्रॉन pad कक्षक में उपस्थित इलेक्ट्रॉन की तुलना में नाभिक से अधिक दृढ़ता से बँधे होते हैं। क्योंकि ऽ कक्षक, p व d कक्षक की तुलना में नाभिक के अधिक पास स्थित होता है। दूसरे शब्दों में sp संकरित कक्षक में 5 गुण (50%), sp2 (33:3%) तथा sp3 संकरित कक्षक (25%) की तुलना में अधिक होता है।
जिसके कारण sp संकरित कार्बन परमाणु sp2तथा sp3 संकरित कार्बन की तुलना में अधिक ऋणविद्युती होता है। जिसके कारण C – Hबंध के इलेक्ट्रॉन कार्बन की ओर विस्थापित होने लगता है। जिसके फलस्वरूप कार्बन पर आंशिक ऋणावेश व हाइड्रोजन पर आंशिक धनावेश आ जाता है और इस प्रकार यह आयनित होकर धनावेशित H+ को प्रोटॉन के रूप में दान कर सकता है। इसलिये यह दुर्बल अम्ल के रूप में कार्य करता है।
उदाहरण –
(1) AgNO3 से अभिक्रिया – एसीटिलीन गैस को अमोनियामय सिल्वर नाइट्रेट के विलयन में प्रवाहित करने पर सिल्वर एसीटीलाइड का श्वेत अवक्षेप प्राप्त होता है। H – C ≡ C – H + 2NH4OH + 2AgNO3 → Ag – C = C – Ag + 2NH4NO3 + 2H2O
(2) अमोनियामय कॉपर क्लोराइड के साथ अभिक्रिया-एसीटिलीन गैस को अमोनियामय क्यूप्रस क्लोराइड के विलयन में प्रवाहित करने पर लाल रंग का क्यूप्रस एसीटीलाइड का अवक्षेप प्राप्त होता है। H – C ≡ C – H + Cu2Cl2 + 2NH4 OH ≡ Cu – C ≡ C – Cu + 2NH4Cl + 2H2O
![]()
प्रश्न 6.
संरूपण से आप क्या समझते हैं ? एथेन के संरूपण का विस्तारपूर्वक वर्णन कीजिए।
उत्तर:
कार्बन-कार्बन एकल बंध के मध्य घूर्णन के कारण जो विभिन्न आकाशीय व्यवस्थाएँ उत्पन्न होती हैं, जिन्हें संरूपी कहते हैं तथा संरूपियों से संबंधित आण्विक ज्यामिति को संरूपण समावयवता कहते हैं। एथेन में संरूपण समावयवता-एथेन में दो कार्बन परमाणु एकल बंध की सहायता से जुड़े रहते हैं तथा प्रत्येक कार्बन पर तीन हाइड्रोजन परमाणु द्वारा जुड़े रहते हैं। अर्थात् एथेन अणु में दो मेथिल समूह एकल बंध की सहायता से जुड़े रहते हैं।
यदि इसमें से एक कार्बन को स्थिर रखते हुए दूसरे कार्बन परमाणु को एकल बंध के चारों तरफ मुक्त घूर्णन करने दिया जाये तो विभिन्न त्रिविम व्यवस्थाएँ संभव हैं। सामान्यतः यदि एक कार्बन को स्थिर रखते हुये दूसरे कार्बन को एकल बंध के चारों तरफ 60° के कोण से मुक्त घूर्णन करने दिया जाये तो मुख्यतः 6 त्रिविम व्यवस्थाएं संभव हैं, जिनमें से 1, 3 और 5 संरचनाएँ समान हैं। इसलिये इनकी ऊर्जा तथा स्थायित्व भी समान होगा। इसी प्रकार 2, 4 और 6 वीं संरचना समान है इसलिये इनकी ऊर्जा तथा स्थायित्व भी समान होगा।
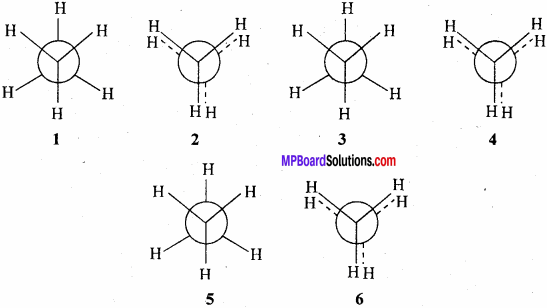
1. सांतरित रूप:
सांतरित रूप में दोनों कार्बन परमाणुओं पर H परमाणु इस प्रकार व्यवस्थित रहते हैं कि उनके बीच दूरी अधिकतम है जिसके कारण इनके बीच लगने वाला प्रतिकर्षण बल न्यूनतम रहता है जिसके फलस्वरूप इनकी ऊर्जा कम तथा स्थायित्व अधिक रहता है।
2. ग्रसित रूप:
ग्रसित रूप में दोनों कार्बन परमाणु इस प्रकार व्यवस्थित रहते हैं कि उनसे जुड़े हाइड्रोजन परमाणु के मध्य न्यूनतम दूरी है जिसके कारण इनके बीच लगने वाला प्रतिकर्षण बल अधिकतम होता है जिसके फलस्वरूप इनकी ऊर्जा अधिकतम तथा स्थायित्व न्यूनतम होता है। एथेन में सांतरित संरूपीय ग्रसित संरूपीय की अपेक्षा 12.6 kJ/mo ऊर्जा से अधिक स्थायी है। यह ऊर्जा का अंतर बहुत कम होने के कारण एथेन में से दोनों संरूपों को पृथक् करना कठिन होता है।
प्रश्न 7.
परॉक्साइड की उपस्थिति में, प्रोपीन में HBr का योग प्रतिमार्कोनीकॉफ नियमानुसार होता है, परन्तु HCl तथा Hl परॉक्साइड प्रभाव प्रदर्शित नहीं करते हैं, क्यों?
उत्तर:
प्रोपीन में HCI तथा HI के योग में परॉक्साइड प्रभाव प्रदर्शित नहीं होता है। इसका कारण है कि H – Cl आबंध (430.5 kJ moll-1), H – Br आबंध (363.7 kJ moll-1) की अपेक्षा प्रबल होने के कारण मुक्त मूलक द्वारा विदलित नहीं हो पाता है। दूसरी ओर H – I आबंध (296-8 kJ mol-1) दुर्बल होता है तथा आयोडीन मुक्त मूलक द्विआबंध में जुड़ने की अपेक्षा आयोडीन अणु से संयुक्त होता है। इसकी ऊष्मागतिकीय आँकड़ों की सहायता से भी व्याख्या की जा सकती है। हाइड्रोजन हैलाइड की मुक्त मूलक योगात्मक अभिक्रियाओं में प्रयुक्त चरणों में एन्थैल्पी परिवर्तन निम्न प्रकार है –
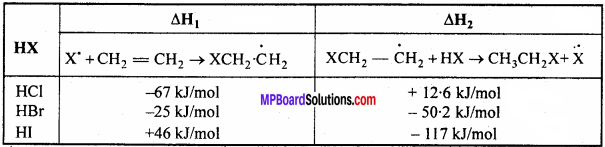
उपरोक्त आँकड़ों से स्पष्ट है कि HBr के योग के दोनों चरण ऊष्माक्षेपी है जो कि अभिक्रिया होने की अनुकूल दशा है। परन्तु HCl तथा HI की दशा में एक चरण ऊष्माशोषी है, जो कि किसी भी रासायनिक अभिक्रिया के होने के लिए ऊष्मागतिकी की दृष्टि से अनुकूलतम स्थिति नहीं है।
प्रश्न 8.
साइक्लोहेक्सेन में संरूपण समावयवता को समझाइये।
उत्तर:
खुली श्रृंखला वाले एल्केनों के अतिरिक्त बंद श्रृंखला वाले साइक्लोएल्केन भी संरूपण समावयवता दर्शाते हैं। साइक्लोप्रोपेन तथा साइक्लोब्यूटेन में बंध कोण क्रमश: 60° तथा 90° का होता है। जिनके कारण ये वलय तनाव में होते हैं तथा इनकी क्रियाशीलता अधिकतम होती है।
साइक्लोपेंटेन में बंध कोण 108° होता है जो कि सामान्य चतुष्फलकीय बंध कोण के निकटतम है। साइक्लोहेक्सेन में बंध कोण 109°28′ होता है। जिसके कारण वलय तनावरहित तथा अधिक स्थायी होती है। इसलिये इसमें संरूपण समावयवता दर्शायी जा सकती है। त्रिविम में विभिन्न व्यवस्थाओं के कारण यह दो समावयवी रूपों में पाया जाता है।
1. कुर्सी संरूपण – यह साइक्लोहेक्सेन का अत्यधिक स्थायी संरूपी है जिसमें सभी बंध कोण चतुष्फलकीय बंध कोण 109°28 के बराबर है। लेकिन समीपवर्ती कार्बन परमाणु के हाइड्रोजन सांतरित स्थिति में है। इसलिये यह वलय तनाव से मुक्त है और इसका स्थायित्व अधिकतम है।
2. नाव संरूपण – यह साइक्लोहेक्सेन का कम स्थायी समावयवी रूप है। इसमें भी सभी बंध कोण चतुष्फलकीय बंध कोण के बराबर है। लेकिन समीपवर्ती कार्बन परमाणु के हाइड्रोजन ग्रसित रूप में है जिसके कारण वलय तनाव में है तथा इसका स्थायित्व कुर्सी रूप की तुलना में कम है। कुर्सी रूप तथा नाव रूप में ऊर्जा का अंतर 44 kJ/mol-1 है।
नाव संरूपण –
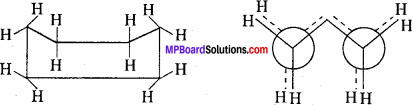
कुर्सी संरूपण –
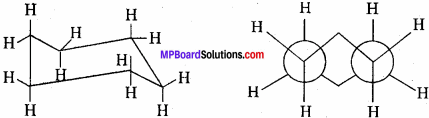
प्रश्न 9.
ऐथेन के ग्रस्त तथा सांतरित रूपों के न्यूमैन तथा साँहार्स प्रक्षेप लिखिए। इनमें से कौन-सा प्रक्षेप अधिक स्थायी होगा तथा क्यों?
उत्तर:
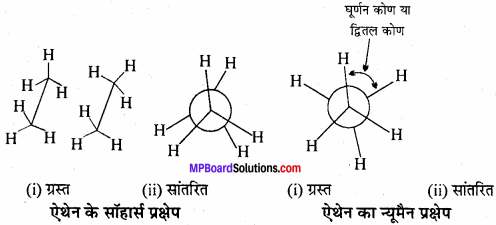
ऐथेन का सांतरित रूप, ग्रस्त रूप की अपेक्षा लगभग 12.5 kJmol-1 ऊर्जा द्वारा अधिक स्थायी होता है। इसका कारण है कि सांतरित रूप में कोई भी दो हाइड्रोजन परमाणु समीपवर्ती कार्बन परमाणुओं से अधिकतम दूरी पर स्थित होते हैं जबकि ग्रस्त अवस्था में ये अत्यधिक पास-पास (कभी-कभी अध्यारोपित भी हो जाते हैं) आ जाते हैं। अतः सांतरित रूप में, इनमें न्यूनतम प्रतिकर्षण बल, न्यूनतम ऊर्जा तथा अधिकतम स्थायित्व होता है।
प्रश्न 10.
ब्यूटेन में संरूपण समावयवता को समझाइये।
उत्तर:
n ब्यूटेन को एथेन का डाइ मेथिल व्युत्पन्न माना जा सकता है जिसमें प्रत्येक कार्बन का एकएक हाइड्रोजन परमाणु मेथिल समूह से प्रतिस्थापित हो गया है। ऐथेन के समान ब्यूटेन में यदि C2 को स्थिर रखकर C3 को घुमाया जाता है तब 360° से घुमाने पर अणु पुनः मूल स्थिति में आ जाता है। जब दोनों कार्बन परमाणु के मेथिल समूह एक-दूसरे से अधिकतम दूरी पर स्थित होते हैं तो इनमें न्यूनतम प्रतिकर्षण होता है तथा सबसे स्थायी रूप है इसे पूर्णतः सांतरित रूप (I) कहते हैं।
पूर्ण सांतरित रूप को घूमाने पर क्रमशः 120° व 240° पर III व V रूप प्राप्त होता है इसमें एक कार्बन का मेथिल समूह दूसरे कार्बन के मेथिल व हाइड्रोजन परमाणु के मध्य होता है। इसे गॉश रूप कहते हैं, यह कम स्थायी होता है। रूप I को 60° व 300° पर घुमाने से क्रमशः II व VI रूप प्राप्त होते हैं ।
ये ग्रसित रूप कहलाता है तथा 180° पर रूप IV प्राप्त होता है जो पूर्णतः ग्रसित रूप है। रूप IV सबसे कम स्थायी है। इसमें दोनों मेथिल समूह की दूरी न्यूनतम होती है। अतः प्रतिकर्षण अधिकतम होता है। पूर्णतः ग्रसित रूप IV की अपेक्षा ग्रसित रूप II व III का स्थायित्व थोड़ा अधिक होता है।
प्रश्न 11.
बेंजीन के अनुनाद सूत्र को समझाइये।
उत्तर:
बेंजीन में प्रत्येक C – Cबंध लंबाई 1.40 A होती है जो कि एकल बंध 154 A और युग्म बंध 134 A के मध्यवर्ती है। अत: बेंजीन में C – C बंध एकल बंध या युग्म बंध से न जुड़े होकर आंशिक युग्म बंध तथा आंशिक एकल बंध से जुड़े होते हैं। अर्थात् कुछ समय पश्चात् द्वि-बंध एकल बंध में तथा एकल बंध द्विबंध में परिवर्तित होते रहते हैं। ऐसे बंधों की कल्पना तो की जा सकती है। लेकिन इन्हें कागजों पर नहीं दर्शाया जा सकता है। इसलिये ऐसा माना जाता है कि बेंजीन निम्नलिखित संरचनाओं का अनुनादी सूत्र है।
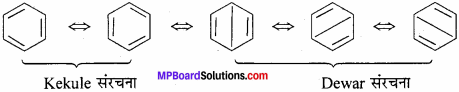
उपर्युक्त संरचनाओं में पहली तथा दूसरी संरचना Kekule संरचना है तथा तीसरी, चौथी तथा पाँचवीं संरचना Dewar संरचना है। Dewar संरचना की ऊर्जा अधिक होती है Para बंध की उपस्थिति के कारण। इसलिये अनुनाद में इनका योगदान केवल 20% होता है। जबकि Kekule सूत्र समतुल्य है और अन्य सूत्र की अपेक्षा अधिक स्थायी है।
इसलिये अनुनाद में इनका योगदान 80% होता है। इसी कारण बेंजीन को इन दो संरचनाओं Kekule सूत्र का ही अनुनादी संकर माना जाता है। सामान्यतः अनुनादी संकर सूत्र को अनेक सूत्र के स्थान पर केवल एक पार्श्व सूत्र द्वारा प्रदर्शित करते हैं जिसमें खंडित वृत्त असंतृप्तता को दर्शाता है।
![]()
प्रश्न 12.
एल्केन में होने वाली हैलोजनीकरण अभिक्रिया की मुक्त मूलक क्रियाविधि को समझाइये।
उत्तर:
एल्केन में हैलोजनीकरण अभिक्रिया मुक्त मूलक क्रियाविधि द्वारा सम्पन्न होती है।
1. श्रृंखला का समारम्भ पद – उच्च ताप या प्रकाश के पराबैंगनी विकिरण की ऊर्जा से क्लोरीन के अणु का समांश विखण्डन होता है एवं क्लोरीन का मुक्त मूलक प्राप्त होता है।
![]()
2. श्रृंखला संचरण पद – उक्त पद में क्लोरीन मुक्त मूलक एल्केन अणु में हाइड्रोजन को विस्थापित कर एक एल्किल मुक्त मूलक प्राप्त होता है।
![]()
यह मुक्त मेथिल मूलक क्लोरीन अणु से क्रिया कर एल्किल हैलाइड तथा क्लोरीन मुक्त मूलक देता है।
![]()
यह मुक्त क्लोरीन मूलक पुनः एल्केन से अभिक्रिया कर मेथिल मूलक देता है। इस प्रकार अभिक्रिया की पुनरावृत्ति होती रहती है।
![]()
3. श्रृंखला का समापन पद – अंत में दोनों मुक्त मूलक परस्पर क्रिया करके श्रृंखला अभिक्रिया को समाप्त कर देते हैं।
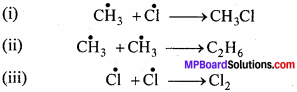
हैलोजन का मुक्त मूलक एल्किल हैलाइड पर आक्रमण कर नया मुक्त मूलक बनाता है।
![]()
यह मुक्त मूलक हैलोजन के साथ क्रिया कर डाइ हैलोएल्केन देता है। यह प्रक्रिया धीरे – धीरे तब तक चलती रहती है जब तक सभी हाइड्रोजन परमाणु क्लोरीन द्वारा प्रतिस्थापित नहीं हो जाते हैं।

प्रश्न 13.
समूहों के दिशात्मक प्रभाव का इलेक्ट्रॉनिक स्पष्टीकरण दीजिए।
उत्तर:
यदि बेंजीन रिंग पर एक प्रतिस्थापी समूह पहले से उपस्थित है तो प्रतिस्थापन अभिक्रिया के फलस्वरूप नया समूह रिंग के किस स्थान पर प्रवेश करेगा इसका निर्धारण पहले से उपस्थित प्रतिस्थापी समूह की प्रकृति के आधार पर होता है इसे उस समूह का दैशिक प्रभाव कहते हैं।
इलेक्ट्रॉनिक सिद्धान्त के आधार पर समूह के निर्देशक प्रभाव की व्याख्या –
1. ऑर्थों व पैरा निर्देशकारी समूह – ये वे समूह होते हैं जो बेंजीन वलय पर पहले से उपस्थित होने पर नये समूह को ऑर्थो व पैरा स्थान पर निर्देशित करते हैं।
उदाहरण – OH, – OCH3, – CH3, – NH2
ये समूह अपनी इलेक्ट्रॉन मुक्तकारी क्षमता के कारण बेंजीन में ऑर्थो व पैरा स्थिति में इलेक्ट्रॉन घनत्व बढ़ा देते हैं। इलेक्ट्रॉन घनत्व बढ़ जाने की वजह से बेंजीन नाभिक की क्रियाशीलता बढ़ जाती है तथा इलेक्ट्रॉन स्नेही अभिकर्मक इस स्थिति में उच्च इलेक्ट्रॉन घनत्व होने के कारण इन्हीं स्थानों पर प्रवेश करता है। .
2. मेटा निर्देशकारी प्रभाव – ये वे समूह हैं जो बेंजीन वलय पर पहले से उपस्थित होने पर नये समूह को मेटा स्थान पर निर्देशित करते हैं।
उदाहरण- – NO2 – COOH, – SO3H, – CN
जब ये समूह बेंजीन वलय पर जुड़े होते हैं तो मेसोमेरिक प्रभाव के कारण बेंजीन वलय से इलेक्ट्रॉन खींच लेते हैं जिसके फलस्वरूप वलय का इलेक्ट्रॉन घनत्व कम हो जाता है तथा इलेक्ट्रॉन घनत्व मुख्यतः ऑर्थो तथा पैरा स्थिति पर घटता है जबकि मेटा स्थिति अप्रभावित रहती है अर्थात् मेटा स्थिति पर इलेक्ट्रॉन घनत्व उच्च रहता है। इसलिये इलेक्ट्रॉन स्नेही अभिकर्मक मेटा स्थिति पर प्रवेश करता है।
प्रश्न 14.
क्लोरीनीकरण के प्रति 1°,2°,3° हैलोजनों की आपेक्षिक क्रियाशीलता 1:3.8:5 है। 2 – मेथिल ब्यूटेन के सभी मोनोक्लोरीनीकृत उत्पादों की प्रतिशतता ज्ञात कीजिए।
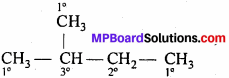
मोनो क्लोरीनीकृत उत्पादों की आपेक्षिक मात्रा = हाइड्रोजन की मात्रा × आपेक्षिक क्रियाशीलता –
(1°) मोनो क्लोरीनीकृत उत्पाद के लिए = 9 × 1 = 9
(2°) मोनो क्लोरीनीकृत उत्पाद के लिए = 2 × 3.8 = 7.6
(3°) मोनो क्लोरीनीकृत उत्पाद के लिए = 1 × 5 = 5
मोनो क्लोरीनीकृत यौगिकों की कुल संख्या = 9 + 7.6 + 5 = 21.6
1° मोनो क्लोरीनीकृत उत्पाद की % मात्रा = \(\frac { 9 × 100 }{ 21.6 }\) = 41.67%
2° मोनो क्लोरीनीकृत उत्पाद की % मात्रा = \(\frac { 7.6 × 100 }{ 21.6 }\) = 35.18%
3° मोनो क्लोरीनीकृत उत्पाद की % मात्रा =\(\frac {5 × 100 }{ 21.6 }\) = 23.15 %
प्रश्न 15.
निम्नलिखित अभिक्रिया के फलस्वरूप कौन-सा उत्पाद प्राप्त होगा तथा क्यों ?
![]()
जब फ्रीडल – क्राफ्ट ऐल्कीकरण उच्च ऐल्किल हैलाइड जैसे n – प्रोपिल क्लोराइड के साथ होता है, तो इलेक्ट्रॉन स्नेही, n – प्रोपिल कार्बधनायन (1° कार्बधनायन) पुनर्व्यवस्थित होकर अधिक स्थायी आइसो-प्रोपिल कार्बधनायन (2° कार्बधनायन) में बदल जाता है तथा अभिक्रिया के परिणामस्वरूप मुख्य उत्पाद आइसो-प्रोपिल बेन्जीन प्राप्त होता है।
![]()
प्रश्न 16.
निम्नलिखित यौगिकों को इलेक्ट्रॉन स्नेही अभिकर्मक के प्रति उनकी घटती हुई आपेक्षिक क्रियाशीलता के क्रम में व्यवस्थित कीजिए।
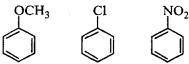
उत्तर:
OCH3 (मेथॉक्सी समूह) इलेक्ट्रॉन निर्मुक्त करने वाला समूह है। यह अनुनाद प्रभाव (+R प्रभाव) के कारण बेन्जीन नाभिक पर इलेक्ट्रॉन घनत्व बढ़ाता है। इसके कारण एनीसॉल, इलेक्ट्रॉन स्नेही अभिकर्मकों के प्रति, बेन्जीन की अपेक्षा अधिक क्रियाशील है। ऐरिल हैलाइडों की दशा में, हैलोजन अपने प्रबल – I प्रभाव के कारण अत्यधिक निष्क्रिय होते हैं जिससे बेन्जीन वलय में कुल इलेक्ट्रॉन घनत्व घट जाता है। इसके कारण पुनः प्रतिस्थापन घट जाता है।
– NO2 समूह इलेक्ट्रॉन आकर्षित करने वाला समूह है। यह प्रबल – प्रभाव के कारण बेन्जीन नाभिक में इलेक्ट्रॉन घनत्व घटाता है। जिसके कारण नाइट्रोबेन्जीन कम क्रियाशील हो जाती है। अतः इन यौगिकों की इलेक्ट्रॉन स्नेही अभिकर्मकों के प्रति कियाशीलता का क्रम निम्न होगा –